cho 13 gam zn tác dụng vừa đủ với 200 gam dung dịch h2so4 loãng a) tính thể tích khí h2 thoát ra ở đkc và khối lượng zn so4 tạo thành sau phản ứng b) tính nồng độ phần trăm dung dịch thu được sau phản ứng
Hóa học
Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
_____0,2______________0,2___0,2 (mol)
a, \(V_{H_2}=0,2.24,79=4,958\left(l\right)\)
\(m_{ZnSO_4}=0,2.161=32,2\left(g\right)\)
b, m dd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
\(\Rightarrow C\%_{ZnSO_4}=\dfrac{32,2}{212,6}.100\%\approx15,15\%\)
Đúng 1
Bình luận (0)
a, \(2CH_3COOH+Mg\rightarrow\left(CH_3COO\right)_2Mg+H_2\)
\(2CH_3COOH+Zn\rightarrow\left(CH_3COO\right)_2Zn+H_2\)
b, Ta có: 24nMg + 65nZn = 4,245 (1)
Theo PT: \(n_{CH_3COOH}=2n_{Mg}+2n_{Zn}=0,2.1=0,2\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,055\left(mol\right)\\n_{Zn}=0,045\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,055.24=1,32\left(g\right)\\m_{Zn}=0,045.65=2,925\left(g\right)\end{matrix}\right.\)
c, \(n_{H_2}=\dfrac{1}{2}n_{CH_3COOH}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
a + b,
MgCl → MgCl2 - Magie clorua
KSO3 → K2SO3 - kali sunfit
CaHCO3 → Ca(HCO3)2 - canxi hidrocacbonat
AlS → Al2S3 - Nhôm sunfua
Đúng 3
Bình luận (0)
a, \(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\)
b, Không pư.
c, \(Fe+CuCl_2\rightarrow FeCl_2+Cu\)
d, \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_4\)
e, \(Ca\left(OH\right)_2+Na_2CO_3\rightarrow2NaOH+CaCO_3\)
f, Không pư
g, \(Na_2SO_3+H_2SO_4\rightarrow Na_2SO_4+SO_2+H_2O\)
h, \(2NH_4Cl+Ba\left(OH\right)_2\rightarrow BaCl_2+2NH_3+2H_2O\)
Đúng 1
Bình luận (0)
viết các pthh sau(ghi rõ đk nếu có) 1.C2H4+O2-> 2.C2H2+O2-> 3.C2H6O+O2-> 4.C2H2+Br2-> 5.CH3COOH+NaOH-> 6.C2H4+Br2-> 7.CH3COOH+Na-> 8.C2H2+Br2->
1. \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
2. \(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
3. \(C_2H_6O+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
4. \(CH\equiv CH+2Br_2\rightarrow CHBr_2-CHBr_2\)
5. \(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
6. \(CH_2=CH_2+Br_2\rightarrow CH_2Br-CH_2Br\)
7. \(2CH_3COOH+2Na\rightarrow2CH_3COONa+H_2\)
8. Giống PT 4
Đúng 2
Bình luận (0)
giúp mình câu 5 với ạ tks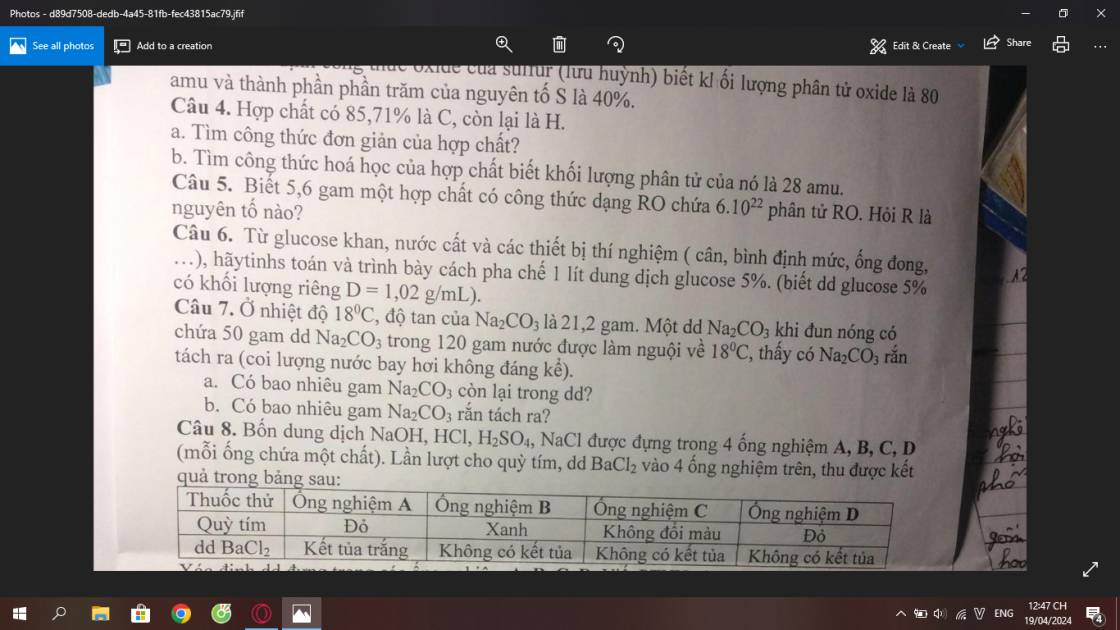
Câu 5:
Ta có: \(n_{RO}=\dfrac{6.10^{22}}{6.10^{23}}=0,1\left(mol\right)\)
\(\Rightarrow M_{RO}=\dfrac{5,6}{0,1}=56\left(g/mol\right)\)
⇒ MR + 16 = 56
⇒ MR = 40 (g/mol)
→ R là Ca.
Đúng 2
Bình luận (0)
Cho m gram A gồm ethanol và phenol phản ứng với Na dư được 3,7185 lít H2 đkc. Mặt khác cho m gram A phản ứng với dung dịch Br2 dư tạo ra 33,1 gram kết tủa. Phần trăm khối lượng của ethanol trong A là
Ta có: nC2H5OH + nC6H5OH = 2nH2 = 0,15.2 (1)
nC6H5OH = nC6H2Br3OH = 0,1 (mol) (2)
Từ (1) và (2) ⇒ nC2H5OH = 0,2 (mol)
\(\Rightarrow\%m_{C_2H_5OH}=\dfrac{0,2.46}{0,2.46+0,1.94}.100\%\approx49,46\%\)
Đúng 2
Bình luận (1)
chọn thuốc thử để phân biệt glucozơ và rượu etylic . viết phương trình minh họa
- Trích mẫu thử.
- Cho từng mẫu thử pư với dd AgNO3/NH3
+ Có tủa trắng bạc: glucozo.
PT: \(C_5H_{11}O_5CHO+2AgNO_3+3NH_3+H_2O\underrightarrow{t^o}C_5H_{11}O_5COONH_4+2NH_4NO_3+2Ag\)
+ Không hiện tượng: rượu etylic.
- Dán nhãn.
Đúng 1
Bình luận (0)
đốt cháy 9,2 gam rượu etylic
a, tính thể tích khí oxi (đktc ) cần dùng
b, thể tích rượu 8 độ thu được khi pha rượu etylic với nước, biết khối lượng riêng của rượu là 0,8g?ml
c, tính khối lượng axit axetic thu được khi lên men lượng rượu trên biết hiệu suất phản ứng là 80%
giúp mình vs ạ
a, Ta có: \(n_{C_2H_5OH}=\dfrac{9,2}{46}=0,2\left(mol\right)\)
PT: \(C_2H_5OH+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
________0,2______0,6 (mol)
\(\Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\)
b, Ta có: VC2H5OH = 9,2:0,8 = 11,5 (ml)
⇒ \(8=\dfrac{11,5}{V_{rượu8^o}}.100\)
⇒ V rượu 8 độ = 143,75 (ml)
c, \(C_2H_5OH+O_2\underrightarrow{^{mengiam}}CH_3COOH+H_2O\)
Theo PT: \(n_{CH_3COOH\left(LT\right)}=n_{C_2H_5OH}=0,2\left(mol\right)\)
Mà: H = 80%
\(\Rightarrow n_{CH_3COOH\left(TT\right)}=0,2.80\%=0,16\left(mol\right)\)
\(\Rightarrow m_{CH_3COOH}=0,16.60=9,6\left(g\right)\)
Đúng 1
Bình luận (0)