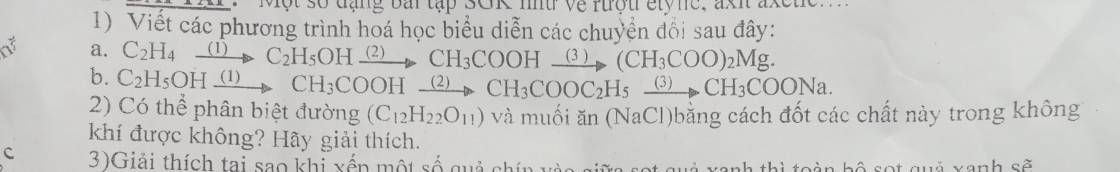
Hóa học
1.
a, (1) \(C_2H_4+H_2O\underrightarrow{^{t^o,xt}}C_2H_5OH\)
(2) \(C_2H_5OH+O_2\underrightarrow{^{mengiam,t^o}}CH_3COOH+H_2O\)
(3) \(2CH_3COOH+Mg\rightarrow\left(CH_3COO\right)_2Mg+H_2\)
b, (1) \(C_2H_5OH+O_2\underrightarrow{^{t^o,mengiam}}CH_3COOH+H_2O\)
(2) \(CH_3COOH+C_2H_5OH⇌CH_3COOC_2H_5+H_2O\) (đk: to, H2SO4 đặc)
(3) \(CH_3COOC_2H_5+NaOH\underrightarrow{t^o}CH_3COONa+C_2H_5OH\)
Đúng 0
Bình luận (0)
Cho 13 g Zn tác dụng hoàn toàn với 200ml dung dịch HCI 2,5M sau phản ứng thu được dung dịch B và khí H a. Tính thể tích khí H, thu được ở đkc b. Tính khối lượng HCI đã phản ứng? c. Tính Cụ các chất trong dung dịch B (coi thể tích dung dịch không đổi)
Tham khảo***
Để giải quyết bài toán này, chúng ta cần sử dụng các bước sau:
**a. Tính thể tích khí H, thu được ở điều kiện chuẩn (đkc):**
Đầu tiên, chúng ta cần phải xác định phản ứng hoá học giữa \( \text{Zn} \) và \( \text{HCl} \):
\[ \text{Zn} + 2\text{HCl} \rightarrow \text{ZnCl}_2 + \text{H}_2 \]
Theo phản ứng này, 1 mol \( \text{Zn} \) tương ứng với 1 mol \( \text{H}_2 \).
Vì vậy, số mol \( \text{H}_2 \) thu được là \( 13 \, \text{mol} \) (vì \( 13 \, \text{g} \) \( \text{Zn} \) đã phản ứng hoàn toàn).
Khí \( \text{H}_2 \) được thu được ở điều kiện chuẩn (đkc) có thể tích tương ứng với số mol đã tính được:
\[ V(\text{H}_2) = n(\text{H}_2) \times 22.4 \, \text{lit} \]
\[ V(\text{H}_2) = 13 \times 22.4 \, \text{lit} = 291.2 \, \text{lit} \]
Vậy, thể tích của khí \( \text{H}_2 \) thu được ở điều kiện chuẩn là \( 291.2 \, \text{lit} \).
**b. Tính khối lượng \( \text{HCl} \) đã phản ứng:**
Ta biết rằng số mol \( \text{H}_2 \) tạo ra trong phản ứng là \( 13 \, \text{mol} \).
Số mol \( \text{HCl} \) ban đầu là:
\[ n(\text{HCl}) = \frac{V(\text{HCl}) \times C(\text{HCl})}{1000} \]
\[ n(\text{HCl}) = \frac{200 \times 2.5}{1000} = 0.5 \, \text{mol} \]
Do đó, số mol \( \text{HCl} \) đã phản ứng là \( 0.5 \, \text{mol} \).
Khối lượng \( \text{HCl} \) đã phản ứng được tính bằng công thức:
\[ m(\text{HCl}) = n(\text{HCl}) \times M(\text{HCl}) \]
\[ m(\text{HCl}) = 0.5 \times 36.5 \]
\[ m(\text{HCl}) = 18.25 \, \text{g} \]
Vậy, khối lượng \( \text{HCl} \) đã phản ứng là \( 18.25 \, \text{g} \).
**c. Tính cụm các chất trong dung dịch B:**
Dung dịch B được tạo ra từ phản ứng giữa \( \text{Zn} \) và \( \text{HCl} \). Sau phản ứng, \( \text{Zn} \) sẽ tan vào dung dịch, tạo ra \( \text{ZnCl}_2 \).
Số mol \( \text{ZnCl}_2 \) được tạo ra bằng với số mol \( \text{Zn} \) đã phản ứng.
Vậy, số mol \( \text{ZnCl}_2 \) là \( 0.5 \, \text{mol} \).
Để tính cụm của các chất trong dung dịch B, ta cần biết thể tích của dung dịch.
Vì không có thông tin về thể tích dung dịch, nên không thể tính được cụm của các chất trong dung dịch B.
Đúng 0
Bình luận (0)
a, Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=0,2.2,5=0,5\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\), ta được HCl dư.
Theo PT: \(n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.24,79=4,958\left(l\right)\)
b, \(n_{HCl\left(pư\right)}=2n_{Zn}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl\left(pư\right)}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{HCl\left(dư\right)}=0,5-0,4=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{HCl\left(dư\right)}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
\(C_{M_{ZnCl_2}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Đúng 0
Bình luận (0)
Dẫn 1,12 lít hỗn hợp gồm etilen và axetilen (đc đo ở đktc) qua dung dịch Brom. Sau khi p/ứ xảy ra hoàn toàn thấy có 12,8 gam Brom đã tham gia a) Viết phương trình p/ứ b) Tính thể tích mỗi khí trong hỗn hợp ban đầu c) Tính thể tích dung dịch brom 0,25M đã dùng ———————— giúp mik với————————
Dẫn 1,12 lít hỗn hợp gồm etilen và axetilen (đc đo ở đktc) qua dung dịch Brom. Sau khi p/ứ xảy ra hoàn toàn thấy có 12,8 gam Brom đã tham gia a) Viết phương trình p/ứ b) Tính thể tích mỗi khí trong hỗn hợp ban đầu c) Tính thể tích dung dịch brom 0,25M đã dùng ———————— giúp mik vs ạ 🥺————————
Muối tạo kết tủa trắng khi cho phản ứng với dung dịch H\(_2\)SO\(_4\) là
chẳng hạn muối BaCl2: Tạo kết tủa trắng BaSO4
BaCl2 + H2SO4 --> BaSO4 + 2HCl
Đúng 1
Bình luận (0)
Phát biểu nào không đúngA.Tất cả các muối Cacbonat(có nhóm CO3) và muối hidrocacbonat(có nhóm -HCO3) đều tác dụng được với dung dịch HCL hoặc CH3COOHB.Trong cùng 1 chu kì,khi đi từ đầu đến cuối chu kì,tính kinh loại tăng dần,tính phi kim giảm dầnC.Dầu mỏ là hỗn hợp phức tạp của nhiều loại hidrocacbon và những lượng nhỏ các hợp chất khác.D.Khi đốt cháy một hợp chất hữu cơ trong khí Oxi thì trong sản phẩm phải có khí Cacbondioxt2.Dãy gồm các chất đều tác dụng với axit axetic là:A.Fe,Na,NaCl,C2H5OH...
Đọc tiếp
Phát biểu nào không đúng
A.Tất cả các muối Cacbonat(có nhóm =CO3) và muối hidrocacbonat(có nhóm -HCO3) đều tác dụng được với dung dịch HCL hoặc CH3COOH
B.Trong cùng 1 chu kì,khi đi từ đầu đến cuối chu kì,tính kinh loại tăng dần,tính phi kim giảm dần
C.Dầu mỏ là hỗn hợp phức tạp của nhiều loại hidrocacbon và những lượng nhỏ các hợp chất khác.
D.Khi đốt cháy một hợp chất hữu cơ trong khí Oxi thì trong sản phẩm phải có khí Cacbondioxt
2.Dãy gồm các chất đều tác dụng với axit axetic là:
A.Fe,Na,NaCl,C2H5OH
B.C2H5OH,KOH,CuO,BaCO3
C.Al,NaOH,C2H5OH,H2SO4
D.Ag,NaOH,C2H5OH,K2CO3
3.0,1 mol khí etilen phản ứng vừa đủ vs 200ml dung dịch Brom aM,vậy 0,1 mol khí axetilen phản ứng tối đa với Vml dung dịch Brom aM.Giá trị của Vml là:
A.200ml
B.300ml
C.400ml
D.100ml
4.Cho các chất :Glucozo,Saccarozo,tinh bột,xenluluzo,chất béo và protein..Số chất đều có công thức tổng quát Cn(H2O)m là
A.4
B.6
C.3
D.5
5.Oxi hóa hoàn toàn 36 gam glucozo (C2H12O6)trong dung dịch AgNO3 dư/NH3(Ag2O) thu được m gam bạc.Tính m gam.Biết (C=12,H=1,O=12,Ag=108)
A.43,2g
B.32,4g
C.21,6g
D.10,8g
6.Cho các chất Saccarozo,tinh bột,xenluluzo và protein.Số chất thủy phân trong môi trường axit,có đun nóng nhẹ(hoặc enzim ở nhiệt độ thường) đều tạo ra glucozo là
A.2
B.3
C.1
D.4
7.Chất tác dụng được với :Na,Na2O,NaOH,Na2CO3,NaHCO3 là
A.axit axetic
B.glucozo
C.rượu etylic
D.etyl axetat
8.Cho 30 gam CH3COOH tác dụng với 92g C2H5OH có H2SO4 đặc làm xúc tác và đun nóng.Biết hiệu suất phản ứng là 60% thì khối lượng etyl axetat tạo thành là
A.176g
B.17,6g
C.26,4g
D.44g
Đốt cháy hoàn toàn 1,68 l hỗn hợp gồm CH4 và C2H2 rồi hấp thụ toàn bộ sản phẩm vào dung dịch Cả(OH)2 trong dư thu 10g kết tủa. a. Viết ptpư b. Nếu dẫn từ từ 3,36 l hỗn hợp trên vào dung dịch brom dư thì khối lượng brom dư là bao nhiêu? giúp em ạ !
Tham khảo:
a. Viết phương trình phản ứng cháy hoàn toàn hỗn hợp CH4 và C2H2:
\[CH_4 + 2O_2 \rightarrow CO_2 + 2H_2O\]
\[C_2H_2 + 2.5O_2 \rightarrow 2CO_2 + H_2O\]
Khi đốt cháy hoàn toàn, tổng số mol \(CO_2\) tạo ra từ cả CH4 và C2H2 sẽ hấp thụ hoàn toàn vào dung dịch Ca(OH)2:
\[CO_2 + Ca(OH)_2 \rightarrow CaCO_3 + H_2O\]
Tính số mol \(CaCO_3\) tạo ra từ phản ứng trên:
- \(n_{CaCO_3} = \frac{m_{CaCO_3}}{M_{CaCO_3}}\)
Sau đó, ta có thể tính số mol \(CH_4\) và \(C_2H_2\) từ số mol \(CaCO_3\) đã biết.
b. Đối với phản ứng với brom, vì \(C_2H_2\) rea đươc hết nên khối lượng brom dư sẽ phụ thuộc vào số mol \(CH_4\) có trong hỗn hợp.
Vậy để tính được khối lượng brom dư, ta cần xác định số mol \(CH_4\) từ số mol \(CaCO_3\) đã tính được ở câu a. Sau đó, sử dụng phương trình phản ứng của \(CH_4\) với brom để tính khối lượng brom cần thiết.
Đúng 0
Bình luận (1)
Hãy nhận biết các chất sau bằng phương pháp hóa học
a) CH₄ , C₂H₂ , CO₂.
b) Rượu Etylic, Axit axetic, dầu đậu nành.
a)
C₂H₂ + 2Br₂ → C2H2Br4
CO₂ + Ca(OH)₂ → CaCO₃ + H₂Ob)
C2H6O + CH₃COOH → CH₃COOC₂H6 + H₂O
CH₃COOH + NaHCO₃ → CH₃COONa + CO₂ + H₂O
C₂H₂ + 2Br₂ → C2H2Br4
CO₂ + Ca(OH)₂ → CaCO₃ + H₂Ob)
C2H6O + CH₃COOH → CH₃COOC₂H6 + H₂O
CH₃COOH + NaHCO₃ → CH₃COONa + CO₂ + H₂O
Đúng 0
Bình luận (1)
Viết PTHH thực hiện các chuyển đổi hóa học sau:
a) CaC₂ → C₂H₂ → C₂H₄ → C₂H₅OH → C₂H₅ONa
b) C₂H₅ →CH₃COOH → CH₃COOK → CH₃COOH → (CH₃COO)₂Cu
c) CH₃COOH → CH₃COOHC₂H₅ → CH₃COONa → CH₄ → CH₃Cl
d) CH₄ → C₂H₂ → C₂H₄ → C₂H₄Br₂
a) CaC₂ + 2H₂O → C₂H₂ + Ca(OH)₂
C₂H₂ + H₂ → C₂H₄
C₂H₄ + H₂O → C₂H₅OH
C₂H₅OH + Na → C₂H₅ONab) C₂H₅OH + O → CH₃COOH
CH₃COOH + KOH → CH₃COOK + H₂O
CH₃COOK + HCl → CH₃COOH + KCl
2CH₃COOH + Cu(OH)₂ → (CH₃COO)₂Cu + 2H₂Oc) CH₃COOH + C₂H₅OH → CH₃COOHC₂H₅ + H₂O
CH₃COOHC₂H₅ + NaOH → CH₃COONa + C₂H₅OH
CH₃COONa + HCl → CH₃COOH + NaCl
CH₃COOH + NaOH → CH₃COONa + H₂O
CH₃COONa + CH₃I → CH₃Cl + CH₃COONad) CH₄ + Cl₂ → CH₃Cl + HCl
CH₃Cl + NaOH → CH₃OH + NaCl
CH₃OH + HBr → CH₃Br + H₂O
C₂H₂ + H₂ → C₂H₄
C₂H₄ + H₂O → C₂H₅OH
C₂H₅OH + Na → C₂H₅ONab) C₂H₅OH + O → CH₃COOH
CH₃COOH + KOH → CH₃COOK + H₂O
CH₃COOK + HCl → CH₃COOH + KCl
2CH₃COOH + Cu(OH)₂ → (CH₃COO)₂Cu + 2H₂Oc) CH₃COOH + C₂H₅OH → CH₃COOHC₂H₅ + H₂O
CH₃COOHC₂H₅ + NaOH → CH₃COONa + C₂H₅OH
CH₃COONa + HCl → CH₃COOH + NaCl
CH₃COOH + NaOH → CH₃COONa + H₂O
CH₃COONa + CH₃I → CH₃Cl + CH₃COONad) CH₄ + Cl₂ → CH₃Cl + HCl
CH₃Cl + NaOH → CH₃OH + NaCl
CH₃OH + HBr → CH₃Br + H₂O
Đúng 0
Bình luận (8)
đốt cháy hoàn toàn 1,38g hợp chất hữu cơ A thu được sản phẩm gồm 2,64g CO2 và 1,62g H2O . Xác định công thức phân tử của A . Biết tỉ khối hơi của A so với Oxi là 1,44
Tham khảo:
Để xác định công thức phân tử của hợp chất hữu cơ \(A\), ta cần thực hiện các bước sau:
1. Xác định số mol của \(CO_2\) và \(H_2O\) được tạo ra:
Số mol \(CO_2\) \(= \frac{2.64 \, \text{g}}{44.01 \, \text{g/mol}}\)
Số mol \(H_2O\) \(= \frac{1.62 \, \text{g}}{18.015 \, \text{g/mol}}\)
2. Xác định số mol của Carbon và Hydrogen trong \(A\) từ sản phẩm \(CO_2\) và \(H_2O\):
Số mol Carbon \(= \frac{2.64 \, \text{g}}{44.01 \, \text{g/mol}}\)
Số mol Hydrogen \(= \frac{2 \times 1.62 \, \text{g}}{18.015 \, \text{g/mol}}\)
3. Xác định tỉ lệ số mol giữa Carbon và Hydrogen trong hợp chất \(A\):
Tỉ lệ số mol \(C : H = \frac{\text{số mol Carbon}}{\text{số mol Hydrogen}}\)
4. Xác định tỉ lệ số mol giữa Carbon và Hydrogen trong hợp chất \(A\) so với tỉ khối hơi của \(A\) so với Oxi:
\(1.44 = \frac{\text{số mol Carbon} \times 12.01 \, \text{g/mol} + \text{số mol Hydrogen} \times 1.008 \, \text{g/mol}}{\text{số mol Carbon} \times 12.01 \, \text{g/mol} + \text{số mol Hydrogen} \times 1.008 \, \text{g/mol} + \text{số mol Oxygen} \times 16.00 \, \text{g/mol}}\)
5. Giải hệ phương trình để tìm số mol Carbon, Hydrogen và Oxygen trong hợp chất \(A\).
6. Xác định công thức phân tử của \(A\) từ số mol của Carbon, Hydrogen và Oxygen.
Hãy thực hiện các bước trên để xác định công thức phân tử của hợp chất \(A\).
Đúng 0
Bình luận (0)




















