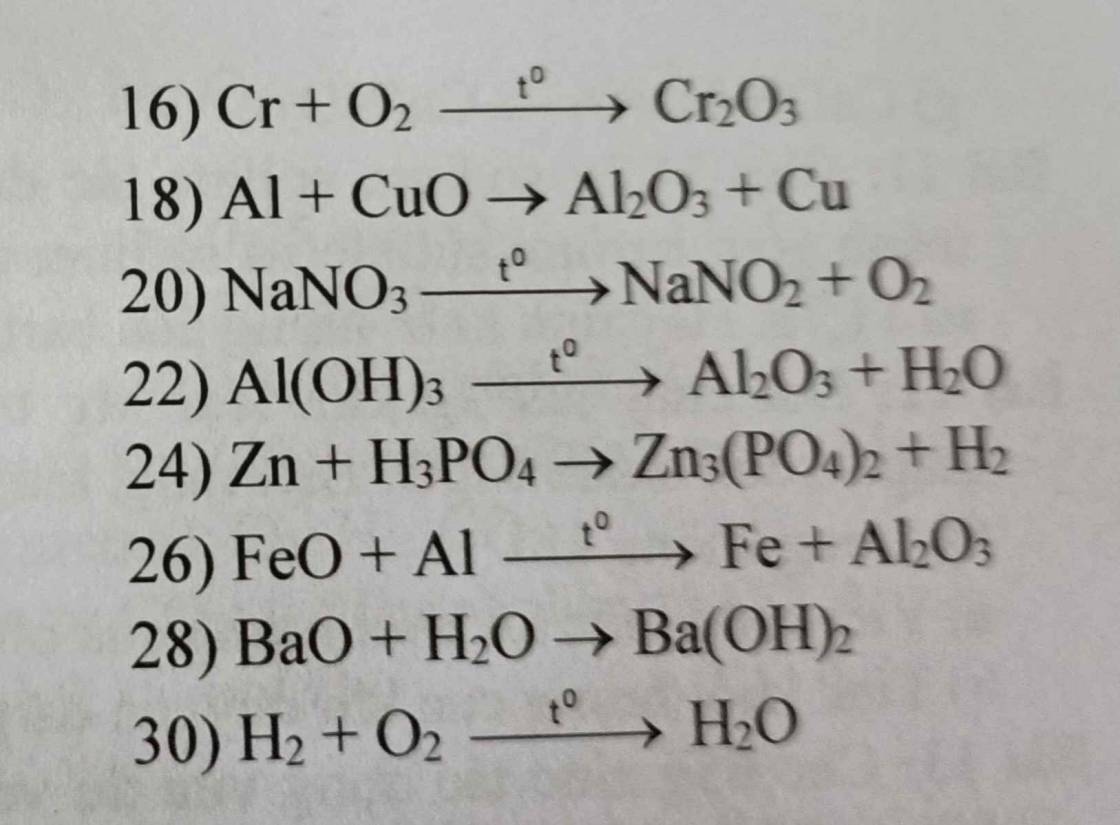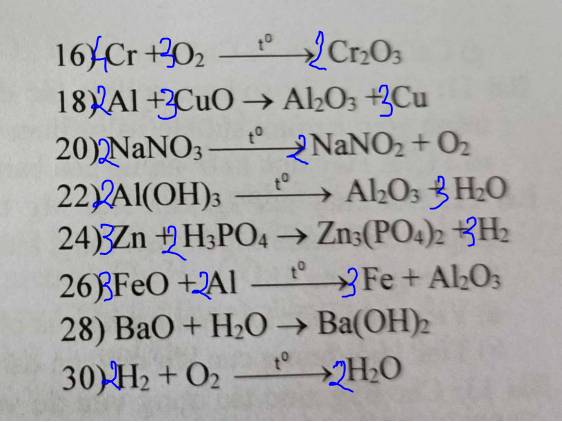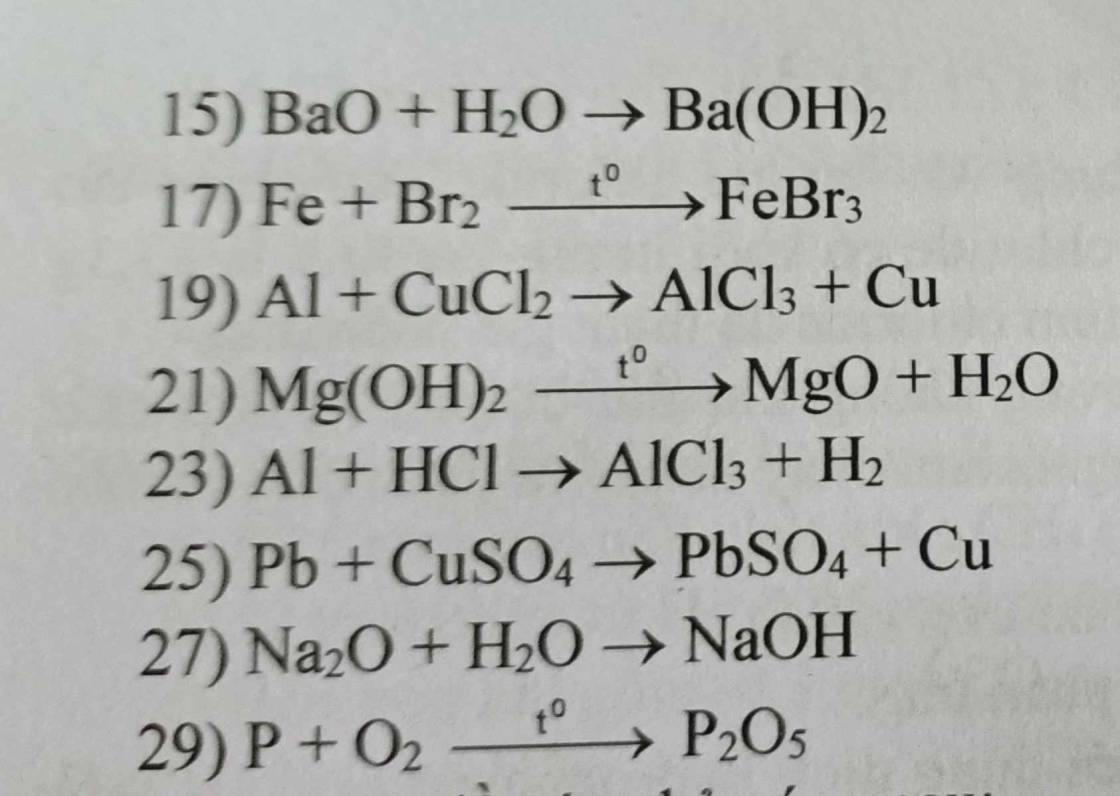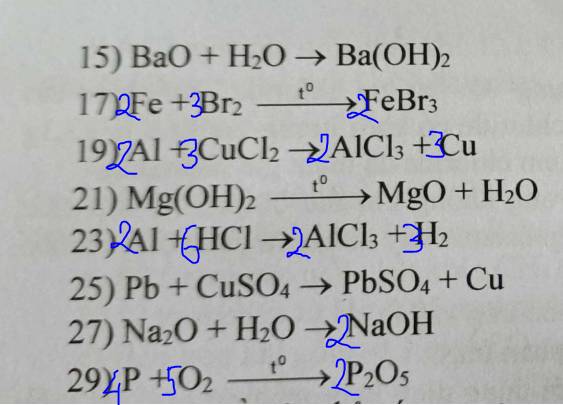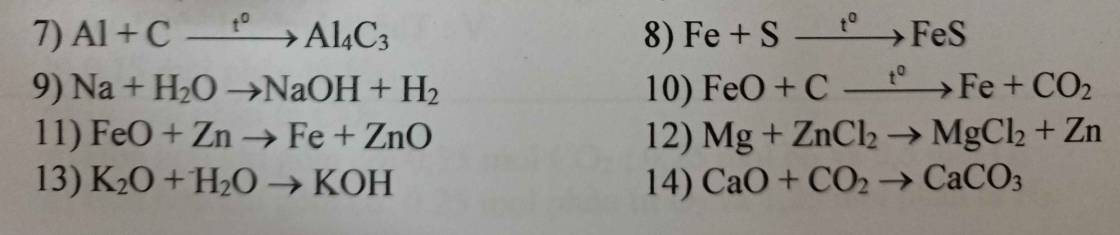tính hàm lượng đạm trong các loại phân bón
a) phân đạm 1 lá (NH4)2 SO4
b) phân đạm 2 lá NH4 NO3
c) phân đạm wrea (NH4)2 CO
Hóa học
a) \(\%N\left(\left(NH_4\right)_2SO_4\right)=\dfrac{28}{132}.100\%=21,21\%\)
b) \(\%N\left(NH_4NH_3\right)=\dfrac{28}{80}.100\%=35\%\)
c) \(\%N\left(\left(NH_4\right)_2CO\right)=\dfrac{28}{60}.100\%\approx46,67\%\)
Đúng 0
Bình luận (0)
Bạn kiểm tra lại đề. Urea có công thức là CO(NH2)2 chứ không có gốc ammonium nhé.
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn CO2 vào 2,5l dung dịch Ca(OH)2 0,04M thu được 8gkết tủa. Tính V
Xem chi tiết
\(n_{Ca\left(OH\right)_2}=2,5\cdot0,04=0,1\left(mol\right)>n_{CaCO_3}=\dfrac{8}{100}=0,08\left(mol\right)\\ TH1:Ca\left(OH\right)_2dư\\ Ca\left(OH\right)_2+CO_2->CaCO_3+H_2O\\ n_{CO_2}=0,08\\ V=1,792L\\ TH2:Ca\left(OH\right)_2hết\\ CaCO_3+CO_2+H_2O->Ca\left(HCO_3\right)_2\\ n_{CO_2}=0,1+\left(0,1-0,08\right)=0,12mol\\ V=2,688L\)
Vậy V nhận 2 nghiệm là 1,792 (L) và 2,688 (L)
Đúng 3
Bình luận (0)
7) \(4Al+3C\underrightarrow{t^o}Al_4C_3\)
8) \(Fe+S\underrightarrow{t^o}FeS\)
9) \(2Na+2H_2O\rightarrow2NaOH+H_2\)
10) \(2FeO+C\underrightarrow{t^o}2Fe+CO_2\)
11) \(FeO+Zn\rightarrow Fe+ZnO\)
12) \(Mg+ZnCl_2\rightarrow MgCl_2+Zn\)
13) \(K_2O+H_2O\rightarrow2KOH\)
14) \(CaO+CO_2\rightarrow CaCO_3\)
Đúng 1
Bình luận (0)
Nung 43,3 gam hỗn hợp gồm KMnO4 và KClO3. Sau một thời gian thu được khí X và chất rắn Y. Nguyên tố Mn chiếm 24,103% khối lượng chất rắn Y. Tính khối lượng của KMnO4 và KClO3 trong hỗn hợp ban đầu. Biết hiệu suất các phản ứng đều đạt 90%.
Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)
Đúng 3
Bình luận (0)
cho nhôm tác dụng hết với 400g dd hcl thấy thoát ra 20,16l h2 a)tính c% của dd hcl đã dùng b)tính c% của dd muối tạo thành sau phản ứng
\(n_{H_2}=\dfrac{20,16}{22,4}=0,9\left(mol\right)\)
PTHH :
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,6 1,8 0,6 0,9
\(a,m_{HCl}=1,8.36,5=65,7\left(g\right)\)
\(C\%_{HCl}=\dfrac{65,7}{400}.100\%=16,425\%\)
\(b,m_{AlCl_3}=0,6.133,5=80,1\left(g\right)\)
\(m_{ddAlCl_3}=\left(0,6.27+400\right)-0,9.2=414,4\left(g\right)\)
\(C\%_{AlCl_3}=\dfrac{80,1}{414,4}.100\%\approx19,33\%\)
Đúng 5
Bình luận (0)
Làm sạch khí CO có lẫn HCl, SO2, CO2 . Viết PTHH
Dẫn hỗn hợp khí qua dung dịch NaOH dư, thu được CO tinh khiết.
\(NaOH+HCl->NaCl+H_2O\\ 2NaOH+SO_2->Na_2SO_3+H_2O\\ 2NaOH+CO_2->Na_2CO_3+H_2O\)
Đúng 3
Bình luận (0)
a. Gọi CTHH của oxit kim loại hóa trị \(III\) là: \(R_2O_3\)
PTPƯ: \(R_2O_3+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2O\)
b. Theo PTPƯ: \(n_{R_2O_3}=n_{R_2\left(SO_4\right)_3}\)
\(\Rightarrow\dfrac{10,2}{M_R.2+48}=\dfrac{34,2}{M_R.2+288}\)
\(\Leftrightarrow5,1\left(M_R+144\right)=17,1\left(M_R+24\right)\)
\(\Leftrightarrow5,1M_R+\text{ 734 , 4}=17,1M_R+410,5\)
\(\Leftrightarrow12M_R=324\)
\(\Leftrightarrow M_R=27\)
Vậy kim loại này là nhôm
\(\Rightarrow\) CTHH: \(Al_3O_2\)
c. \(n_{Al_3O_2}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{Al_2O_3}.3=0,1.3=0,3\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{29,4.100}{20}=147\left(g\right)\)
d. \(V_{ddH_2SO_4}=\dfrac{m}{D}=\dfrac{147}{0,143}=128,61\left(ml\right)\)
Đúng 2
Bình luận (1)
Để hòa tan hoàn toàn 2,4g một oxit kim loại hóa trị II cần dùng 10g dd HCl 21,9% . Hỏi đó là oxit của kim loại nào?(chi tiết)
Gọi CTHH của oxit kim loại là RO
\(m_{HCl}=\dfrac{10.21,9\%}{100\%}=2,19\left(g\right)\\ n_{HCl}=\dfrac{2,19}{36,5}=0,06\left(mol\right)\\ RO+2HCl\xrightarrow[]{}RCl_2+H_2O\\ n_{RO}=\dfrac{0,06}{2}=0,03\left(mol\right)\\ M_{RO}=\dfrac{2,4}{0,03}=80\left(g/mol\right)\\ M_R=80-16=64\left(g/mol\right)\\ \Rightarrow R.là.đồng,Cu\)
Đúng 3
Bình luận (0)