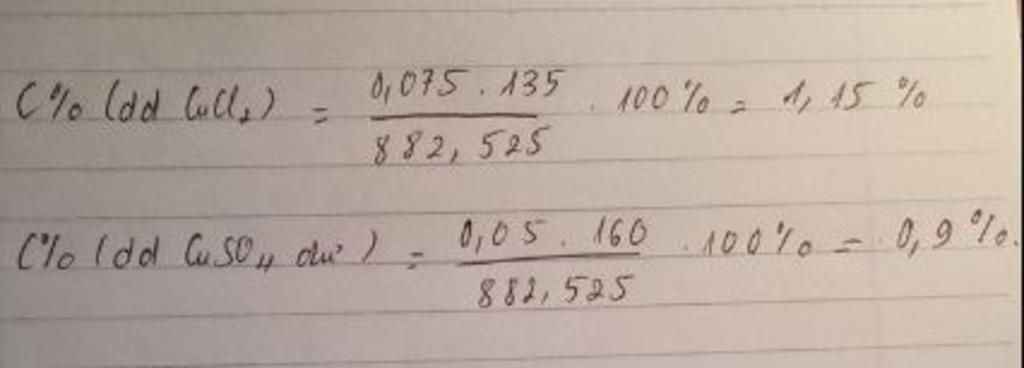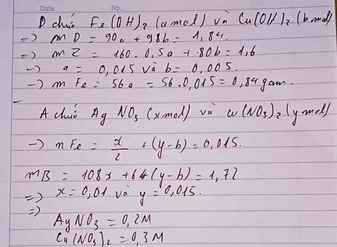Cho 11,2 g Fe vào bình chứa Cl2 dư, sau phản ứng cho m (g) muối. Tính m ?
Hóa học
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ n_{FeCl_3}=n_{Fe}=0,2\left(mol\right)\\ \Rightarrow m_{FeCl_2}=162,5.0,2=32,5\left(g\right)\\ \Rightarrow m=32,5\left(g\right)\)
Đúng 6
Bình luận (0)
Cho 3,2g oxi hoàn toàn với khí hiđrô,sau phản ứng thu được sản phẩm là nước
a,viết phương trình hoá học B,tính thể tích khí hiđrô cần dùng
C,tỉ khối lượng nước tạo thành sau phản ứng
d,cho khí oxi tác dụng với 3,6 khí hiđrô sau pu chất nào còn dư , dư bao nhiêu MOL
a. PTHH: \(2H_2+O_2\rightarrow2H_2O\)
b. \(n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
Theo PTHH: \(n_{H_2}=n_{O_2}\cdot\dfrac{2}{1}=0,1\cdot\dfrac{2}{1}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c. Chưa hiểu đề bài lắm :))
d. Ta có: \(n_{O_2}=0,1\left(mol\right);n_{H_2}=\dfrac{3,6}{22,4}\approx0,16\left(mol\right)\)
Do \(0,1< 0,16\) nên \(H_2\) dư \(0,16-0,1=0,06\left(mol\right)\)
Đúng 2
Bình luận (2)
\(n_{KMnO_4}=1\left(mol\right)\\ a,2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\uparrow\\ a,n_{O_2}=\dfrac{n_{KMnO_4}}{2}=\dfrac{1}{2}=0,5\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,5.22,5=11,2\left(l\right)\\ \Rightarrow V_{kk}=5.V_{O_2\left(đktc\right)}=5.11,2=56\left(l\right)\\ b,2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ n_{MgO}=2.n_{O_2}=2.0,5=1\left(mol\right)\\ \Rightarrow m_{MgO}=1.40=40\left(g\right)\)
Đúng 4
Bình luận (0)
a. PTHH: \(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
- Theo PTHH ta có:
\(n_O=n_{KMnO_4}\cdot\dfrac{1}{2}=1\cdot\dfrac{1}{2}=0,5\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,5.22,4=11,2\left(l\right)\)
- Do thể tích Oxi chiếm 1/5 thể tích không khí nên:
\(V_{KK}=11,2.5=56\left(l\right)\)
Đúng 2
Bình luận (0)
2. Nhiệt phân MgCO3 1 thời gian , ngt thu dược chất rắn A và khí B . Hấp thụ khí B hoàn toàn vào NaOh thu được dd C . Dd C td với cả BaCl2 và dd KOH . Khi cho chất rắn A t/d với dd HCl lại thấy có khí B bay ra.
a. Cho biết chất A , khí B , dd C là gì/
b. Viết pthh của p/ứ xảy ra
a)
Rắn A: MgO và MgCO3 dư( do rắn A tác dụng HCl có khí B bay ra nên MgCO3 có dư)
Khí B: CO2
ddC có dd Na2CO3 và dd NaHCO3 (có NaHCO3 vì dd C có tác dụng dd KOH)
b) Các PTHH:
\(MgCO_3\rightarrow\left(t^o\right)MgO+CO_2\uparrow\\ MgO+2HCl\rightarrow MgCl_2+H_2O\\ MgCO_3+2HCl\rightarrow MgCl_2+CO_2\uparrow+H_2O\\ CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\\ NaOH+CO_2\rightarrow NaHCO_3\\ Na_2CO_3+Ba\left(OH\right)_2\rightarrow BaCO_3\downarrow+2NaOH\\2KOH+2NaHCO_3\rightarrow K_2CO_3+Na_2CO_3+2H_2O\\ 2NaHCO_3+Ba\left(OH\right)_2\rightarrow BaCO_3\downarrow+Na_2CO_3+2H_2O\)
Đúng 3
Bình luận (0)
1.Cho 500g dd BaCl2 3,12% td với 400g dd Cúo4 5% thu được dd A và kết tủa B . Tính k/lg kết tủa B và nồng độ % của các chất trong dd A?
PHIẾU HỌC TẬP TÌM HIỂU BÀI AXIT AXETIC STT Thí nghiệm Hiện tượng-PTHH 1 Nhúng quì tím vào dd axit axetic 2 Cho mẩu magie vào dung dịch axit axetic. 3 Nhỏ dd NaOH vào ống nghiệm, thêm phenolphthalein, nhỏ dd axit axetic vào dd. 4 Nhỏ dd NaOH vào ống nghiệm, thêm phenolphthalein, nhỏ dd axit axetic vào dd. 5 Nhỏ dung dịch axit axetic vào CuO 6 Nhỏ từ từ dung dịch axit axetic vào Na2CO3
Đọc tiếp
PHIẾU HỌC TẬP TÌM HIỂU BÀI AXIT AXETIC
STT | Thí nghiệm | Hiện tượng-PTHH |
1 | Nhúng quì tím vào dd axit axetic
|
|
2 | Cho mẩu magie vào dung dịch axit axetic.
|
|
3 | Nhỏ dd NaOH vào ống nghiệm, thêm phenolphthalein, nhỏ dd axit axetic vào dd.
|
|
4 | Nhỏ dd NaOH vào ống nghiệm, thêm phenolphthalein, nhỏ dd axit axetic vào dd.
|
|
5 | Nhỏ dung dịch axit axetic vào CuO
|
|
6 | Nhỏ từ từ dung dịch axit axetic vào Na2CO3
|
|
STT | Thí nghiệm | Hiện tượng-PTHH |
1 | Nhúng quì tím vào dd axit axetic
| Quỳ tím hoá đỏ |
2 | Cho mẩu magie vào dung dịch axit axetic.
| - Hiện tượng: Mẩu Magie tan trong dung dịch axit axetic, tạo thành dung dịch, có khí không màu thoát ra sau phản ứng \(PTHH:Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2\uparrow\) |
3 | Nhỏ dd NaOH vào ống nghiệm, thêm phenolphthalein, nhỏ dd axit axetic vào dd.
| - Hiện tượng: Sau khi nhỏ thêm phenolphtalein thì dung dịch chuyển sang màu hồng. Sau khi thêm dung dịch axit axetic vào thì dung dịch mất màu hồng. \(PTHH:NaOH+CH_3COOH\rightarrow CH_3COONa+H_2O\) |
4 | Nhỏ dd NaOH vào ống nghiệm, thêm phenolphthalein, nhỏ dd axit axetic vào dd.
| Này giống thì nghiệm 3 em nè |
5 | Nhỏ dung dịch axit axetic vào CuO
| - Hiện tượng: CuO tan trong dung dịch axit axetic tạo thành dung dịch. \(PTHH:CuO+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Cu+H_2O\) |
6 | Nhỏ từ từ dung dịch axit axetic vào Na2CO3
| - Hiện tượng: Sau phản ứng thấy có sủi bọt khí. \(PTHH:Na_2CO_3+2CH_3COOH\rightarrow2CH_3COONa+CO_2\uparrow+H_2O\) |
Đúng 4
Bình luận (7)
Đọc tiếp
a: \(n_{NaCl}=\dfrac{5.85}{58,5}=0.1\left(mol\right)\)
b: \(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
Đúng 1
Bình luận (0)
Một oxit nitơ (X) chứa 30,43% N về khối lượng .Tỉ khối của X so với không khí là 1,5862.Cần bao nhiêu gam dd H N O 3 HNO3 40% tác dụng với Cu để điều chế 1 lit khí X (ở 134 o 134o C,1atm), giả sử phản ứng chỉ giải phóng duy nhất khí X? 13,4g 9,45g 12,3g kết quả khác.
\(n_X=\dfrac{P.V}{R.T}=\dfrac{1.1}{0,082.\left(273+134\right)}=0,03\left(mol\right)\\ M_X=29.1,5862=46\left(\dfrac{g}{mol}\right)\\ Đặt.CTTQ:N_kO_t\left(k,t:nguyên,dương\right)\\ Ta.có:k:t=\dfrac{30,43\%}{14}:\dfrac{69,57\%}{16}=0,022:0,043=1:2\\ \Rightarrow k=1;t=2\\ \Rightarrow CTHH.X:NO_2\\ Cu+4HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ n_{HNO_3}=\dfrac{4}{2}.n_{NO_2}=\dfrac{4}{2}.0,03=0,06\left(mol\right)\\ \Rightarrow m_{ddHNO_3}=\dfrac{0,06.63.100}{40}=9,45\left(g\right)\)
Đúng 1
Bình luận (0)
Lắc m gam bột Fe với dung dịch A gồm AgNO3 và Cu(NO3)2 đến khi phản ứng kết thúc thu được x gam chất rắn B. Tách B thu được nước lọc C. CHo nước lọc C tác dụng với dd NaOH dư thu được a gam kết tủa của 2 Hidroxit kim loại. Nung kết tủa trong kk đến khối lượng không đổi thu được b gam chất rắn. 1. Lập biểu thức tính m theo a và b. 2.Cho a=36,8; b=32; x= 34,4 gam. Tính giá trị m
Theo 6,5g zn tác dụng với Hcl a. Tính khối lượng axit tham gia b. Tính khối lượng zncl2 thu được c. Với lượng khí H2 trên tác dụng với bao nhiêu g Fe2O3
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{HCl}=2.n_{Zn}=2.0,1=0,2\left(mol\right)\\a, \Rightarrow m_{HCl}=0,2.36,5=7,3\left(g\right)\\ b,n_{H_2}=_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\Rightarrow m_{ZnCl_2}=136.0,1=13,6\left(g\right)\\ c,Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\\ n_{Fe_2O_3}=\dfrac{n_{H_2}}{3}=\dfrac{0,1}{3}=\dfrac{1}{30}\left(mol\right)\\ \Rightarrow m_{Fe_2O_3}=\dfrac{1}{30}.160=\dfrac{16}{3}\left(g\right)\)
Đúng 1
Bình luận (0)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
a: \(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(\Leftrightarrow n_{ZnCl_2}=0.1\left(mol\right)\)
\(\Leftrightarrow n_{HCl}=0.2\left(mol\right)\)
\(m_{HCl}=0.2\cdot36.5=7.3\left(g\right)\)
b: \(m_{ZnCl_2}=0.1\cdot136=13.6\left(g\right)\)
Đúng 1
Bình luận (0)