trình bầy các phương trình hóa học H3để phân biệt 4 dd đựng trong 4 bình riêng Cbiệt không có nhãn : HCL; (RCOO)3; C3H5( tan trong rượu etylic); ( CH3COOH); (C2H5OH)
Hóa học
Nêu nhận định của em về sản lượng và giá thành khi sản xuất Oxi trong phòng thí nghiệm và trong công nghiệp.
Trong phòng thí nghiệm: giá thành cao, sản lượng sản xuất ít
Trong công nghiệp: giá thành thấp, sản lượng sản xuất nhiều
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 13,8g 1 hợp chất A,sau pứ thu được 13,44 lít co2 và 16,2g h20
a) xác định ctpt a ,biết d A/h2=23
Do đốt cháy A thu được sản phẩm chứa C, H, O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\) => nC = 0,6 (mol)
\(n_{H_2O}=\dfrac{16,2}{18}=0,9\left(mol\right)\) => nH = 1,8 (mol)
Xét mC + mH = 0,6.12 + 1,8.1 = 9 (g) < 13,8
=> A chứa C,H,O
\(n_O=\dfrac{13,8-9}{16}=0,3\left(mol\right)\)
Xét nC : nH : nO = 0,6 : 1,8 : 0,3 = 2 : 6 : 1
=> CTPT: (C2H6O)n
Mà MA = 23.2 = 46 (g/mol)
=> n = 1
=> CTPT: C2H6O
Đúng 1
Bình luận (2)
Bạn ơi check lại đề giúp mình với!
Đúng 0
Bình luận (1)
cho 6,5 g kẽm tác dụng với dung dịch loãng chứa 14,6 g axit clohidric thu được kẽm clorua và khí hidro
a.viết các phương trình phản ứng xảy ra
b.sau phản ứng chất nào dư và dư bao nhiêu mol \
c. tính thể tích của khí hidro
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 < 0,4 ( mol )
0,1 0,2 0,1 ( mol )
Chất dư là HCl
\(n_{HCl\left(dư\right)}=0,4-0,2=0,2mol\)
\(V_{H_2}=0,1.22,4=2,24l\)
Đúng 1
Bình luận (0)
cho 0,5 lít đ rượu etylic 30 độ pứ với na dư,sau pứ thu được bao nhiêu lít h2,cho biết d rượu=0,8,d nước =1
\(V_{C_2H_5OH\left(nguyên.chất\right)}=\dfrac{0,5.30}{100}=0,15l\)
\(0,15lít=150ml\)
\(V_{H_2O}=500-150=350ml\)
\(m_{C_2H_5OH\left(nguyên.chất\right)}=150.0,8=120g\)
\(m_{H_2O}=350.1=350g\)
\(n_{C_2H_5OH}=\dfrac{120}{46}=2,6mol\)
\(n_{H_2O}=\dfrac{350}{18}=19,44mol\)
\(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\)
2,6 1,3 ( mol )
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
19,44 9,72 ( mol )
\(V_{H_2}=\left(1,3+9,72\right).22,4=246,848l\)
Đúng 1
Bình luận (0)
Đọc tiếp
\(a,SO_2+H_2O\rightarrow H_2SO_3\\
2K+2H_2O\rightarrow2KOH+H_2\\
CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(b,CuO+H_2\underrightarrow{t^O}Cu+H_2O+Cu\\
Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
Đúng 1
Bình luận (0)
Cho 6,9 g na vào 100ml dd hcl 0,1M tìm cM và C% dd sau pư biet d nước = 1 g/ ml , Dhcl = 1,2 g/ ml
\(n_{Na}=\dfrac{6,9}{23}=0,3mol\)
\(n_{HCl}=0,1.0,1=0,01mol\)
\(2Na+2HCl\rightarrow2NaCl+H_2\)
0,3 < 0,01 ( mol )
0,01 0,01 0,01 ( mol )
\(m_{HCl}=0,01.36,5=0,365g\)
\(m_{NaCl}=0,01.58,5=0,585g\)
\(m_{ddspứ}=0,365+6,9-0,01.2=7,245g\)
\(C\%_{NaCl}=\dfrac{0,585}{7,245}.100=8,07\%\)
\(C_{M_{NaCl}}=\dfrac{0,01}{0,1}=0,1M\)
Đúng 2
Bình luận (0)
Đọc tiếp
Câu 4 :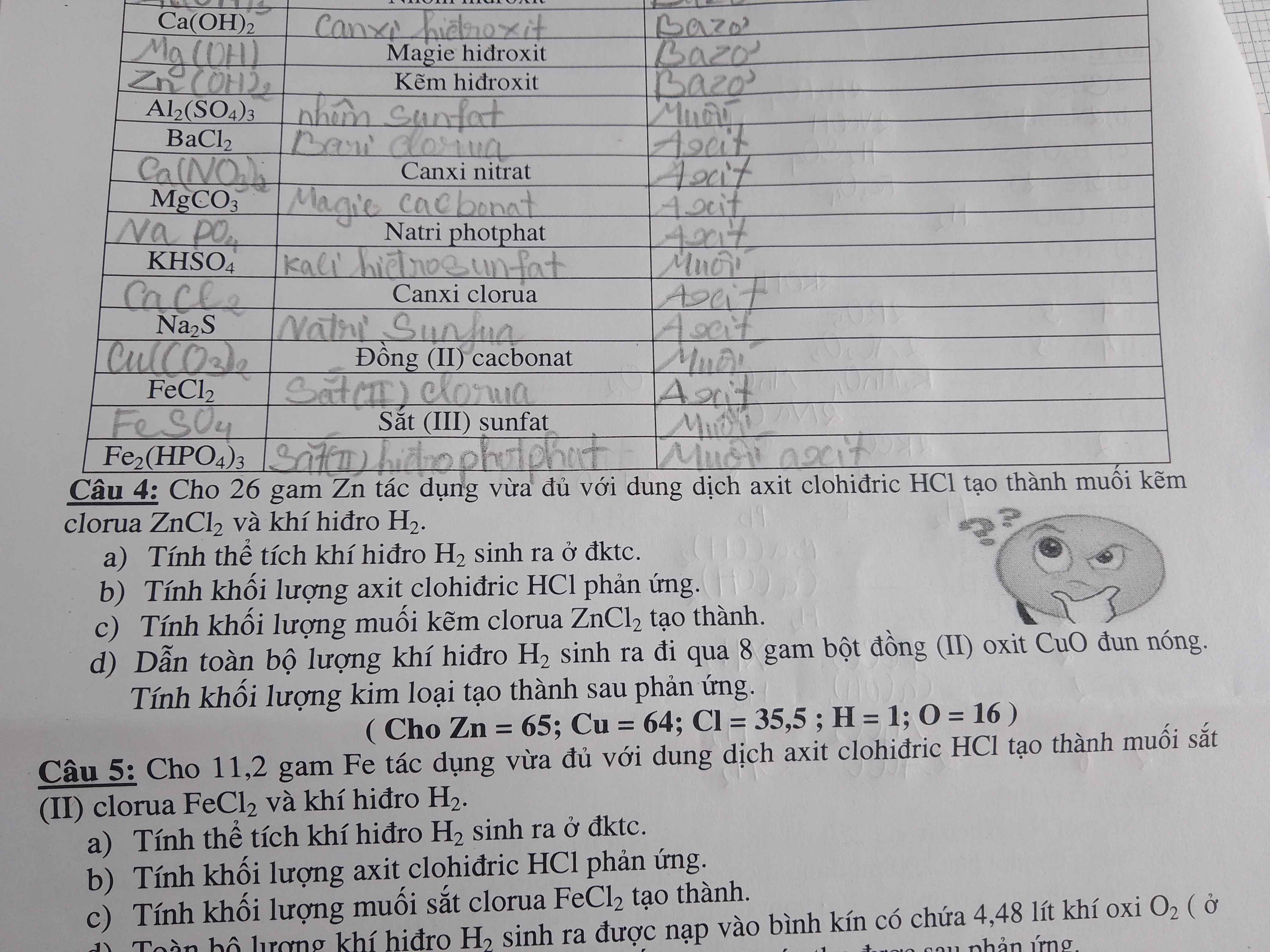
a.b.c.\(n_{Zn}=\dfrac{26}{65}=0,4mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,4 0,8 0,4 0,4 ( mol )
\(V_{H_2}=0,4.22,4=8,96l\)
\(m_{HCl}=0,8.36,5=29,2g\)
\(m_{ZnCl_2}=0,4.136=54,4g\)
d.\(n_{CuO}=\dfrac{8}{80}=0,1mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,1 < 0,4 ( mol )
0,1 0,1 ( mol )
\(m_{Cu}=0,1.64=6,4g\)
Đúng 1
Bình luận (0)
Hòa tan 3,1 gam Na2O vào một lượng nước, rồi thêm nước cho đủ 250ml. Tính nồng độ mol của chất tan thu được. (làm ơn giải chi tiết giúp mình với ạ, cảm ơn mọi người)
250ml = 0,25 lít
\(n_{Na_2O}=\dfrac{3,1}{62}=0,05mol\)
\(Na_2O+H_2O\rightarrow2NaOH\)
0,05 0,1 ( mol )
\(C_{MNaOH}=\dfrac{0,1}{0,25}=0,4M\)
Đúng 2
Bình luận (0)















