HÃY TÍNH SỐ MOL CỦA CÁC SỐ SAU:
8,428.1022 nguyên tử Fe; 1,505.1024 phân tử SO3
HÃY TÍNH SỐ MOL CỦA CÁC SỐ SAU:
8,428.1022 nguyên tử Fe; 1,505.1024 phân tử SO3
\(n_{Fe}=\dfrac{8,428.10^{22}}{6,022.10^{23}}\approx0,14\left(mol\right)\)
\(n_{SO_3}=\dfrac{1,505.10^{24}}{6,022.10^{23}}\approx2,5\left(mol\right)\)
Một số giáo viên hay học sinh khi làm bài tập vẫn viết phản ứng như sau:
\(MgCl_2+2NH_3+2H_2O\rightarrow Mg\left(OH\right)_2+2NH_4Cl\)
Theo em phản ứng trên có hợp lý ở mặt thực tiễn hay không và vì sao?
Hm thưởng thì mình chưa biết :))
Các số liệu hay dẫn chứng để chứng minh cho bài làm của mình các bạn đều có thể tự tìm và trích dẫn lại là được nhé!
- Phản ứng MgCl2 + 2NH3 + 2H2O → Mg(OH)2 + 2NH4Cl không hợp lý trong mặt thực tiễn. Các lý do bao gồm:
+ Không thể xảy ra tự nhiên: Phản ứng này không phù hợp với các quy tắc và nguyên tắc cơ bản của hoá học. Trong môi trường nước, MgCl2 sẽ tạo thành ion Mg2+ và Cl-, còn NH3 sẽ tạo thành ion NH4+ và OH-. Do đó, phản ứng trên không thể xảy ra tự nhiên.
+ Không tuân theo quy tắc bảo toàn nguyên tố: Phản ứng trên không tuân theo quy tắc bảo toàn nguyên tố. Trong phản ứng, nguyên tố Cl trong MgCl2 biến mất và không xuất hiện trong sản phẩm, trong khi nguyên tố N trong NH3 không được tạo ra.
+ Thiếu thông tin chi tiết: Phản ứng trên không cung cấp đủ thông tin chi tiết về điều kiện phản ứng, nhiệt độ, áp suất và chất xúc tác. Các yếu tố này có thể ảnh hưởng đáng kể đến khả năng xảy ra của phản ứng.
Anh là giáo viên vậy anh có viết vậy không? Vì sao? Thưởng thì ko có ạ.
a] nguyên tử A có tổng số hạt là 42 Trong đó số hạt không mang điện là 12 hạt số hạt trong mỗi nguyên tử a
b] vẽ mô hình nguyên tử a
`#3107.101107`
`a)`
Gọi số hạt proton, neutron, electron trong nguyên tử A lần lượt là `p, n, e`
Tổng số hạt trong nguyên tử là `42`
`=> p + n + e = 42`
Mà trong nguyên tử, số `p = e` (nguyên tử trung hòa về điện)
`=> 2p + n = 42`
Vì số hạt không mang điện là `12`
`=> 2p + 12 = 42`
`=> 2p = 42 - 12`
`=> 2p = 30`
`=> p = 30 \div 2`
`=> p = 15`
`=> p = e = 15`
Vậy, số hạt trong nguyên tử A là `p = e = 15.`
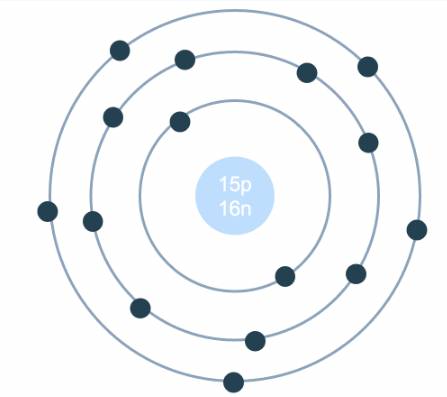
`b)`
Bạn tham khảo hình ảnh mô hình nguyên tử:
a] Ta có:
\(p+e+n=42\)
mà \(p=e\)
\(\Leftrightarrow2p+n=42\\ \Leftrightarrow2p+12=42\\ \Leftrightarrow p=e=15\)
A là P
b]
Gọi: \(\left\{{}\begin{matrix}n_{Fe_2O_3}=x\left(mol\right)\\n_{CuO}=y\left(mol\right)\end{matrix}\right.\) ⇒ 160x + 80y = 16 (1)
\(n_{HCl}=0,55.1=0,55\left(mol\right)\)
\(n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
BTNT H, có: nHCl = 2nH2O + 2nH2 ⇒ nH2O = 0,25 (mol)
BTNT O, có: 3nFe2O3 + nCuO = nH2O ⇒ 3x + y = 0,25 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,05\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{0,05.160}{16}.100\%=50\%\\\%m_{CuO}=50\%\end{matrix}\right.\)
Dd Y gồm: FeCl3: 0,1 (mol) và CuCl2: 0,1 (mol)
Dd Z gồm: FeCl2 và ZnCl2
Chất rắn T gồm: Cu, Fe
BTNT Cu: nCu = nCuCl2 = 0,1 (mol)
Ta có: \(n_{Fe\left(OH\right)_2}=\dfrac{4,5}{90}=0,05\left(mol\right)\)
BTNT Fe, có: nFeCl2 = 0,05 (mol) ⇒ nFe = 0,1 - 0,05 = 0,05 (mol)
BT e, có: 2nZn = 2nH2 + 2nCu + 3nFe + 2nFeCl2
⇒ nZn = 0,25 (mol)
⇒ m = 0,25.65 = 16,25 (g)
nhỏ dung dịch phenolphalein vào ống nghiệm đựng dung dịch sodium hydroxide, sau đó nhỏ tiếp dung dịch nitrics acid hno3 đến dư vào
- Hiện tượng: Khi nhỏ pp vào dd NaOH, thấy dd chuyển hồng. Sau khi nhỏ HNO3 đến dư vào, dd nhạt màu rồi trong suốt.
PT: \(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
Ascobic acid (vitamin C) là một acid hũu cơ được kí hiệu đơn giản là HAsc, phân tử khối là 176 . Một học sinh hoà tan 5,0 g ascorbic acid vào 250 mL nước theo phương trình cân bằng sau: HAsc -><- H cộng + Asc trừ. Ka = 8.10^-5
a/ Tính nồng độ HAsc tại thời điểm cân bằng
b/ Tính pH của dung dịch thu được.
a, \(n_{HAsc}=\dfrac{5}{176}\left(mol\right)\Rightarrow\left[HAsc\right]=\dfrac{\dfrac{5}{176}}{0,25}=\dfrac{5}{44}\left(M\right)\)
PT: \(HAsc⇌H^++Asc^-\)
Bđ: 5/44 0 0 (M)
Pư: x x x (M)
Cb: 5/44-x x x (M)
Có: \(K_a=\dfrac{\left[H^+\right]\left[Asc^-\right]}{\left[HAsc\right]}\) \(\Rightarrow\dfrac{x.x}{\dfrac{5}{44}-x}=8.10^{-5}\Rightarrow x\approx2,975.10^{-3}\left(M\right)\)
\(\Rightarrow\left[HAsc\right]_{cb}\approx0,111\left(M\right)\)
b, \(pH=-log\left[H^+\right]\approx2,53\)
Hoà tan 2,7g Al ACl+6HCl=2AlCl3+3H2 T a.Tính khối lượng HCl b.Thể tích H2 ở 25°C,1bar
\(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PTHH : \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1---->0,3------------------>0,15
a) \(m_{HCl}0,3.36,5=10,95\left(g\right)\)
b) \(V_{H2\left(25^oC,1bar\right)}=0,15.24,79=3,7185\left(l\right)\)
\(a.n_{Al}=\dfrac{2,7}{27}=0,1mol\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ n_{HCl}=\dfrac{0,1.6}{2}=0,3mol\\ m_{HCl}=0,3.36,5=10,59g\\ b.n_{H_2}=\dfrac{0,1.3}{2}=0,15mol\\ V_{H_2,đkc}=0,15.24,79=3,7185l\)
HCl có hóa trị là mấy
Trong hợp chất \(HCl\) , nguyên tử \(Clo\left(Cl\right)\) liên kết với một nguyên tử \(hydro\left(H\right)\)
\(\Rightarrow\) Hóa trị của \(Clo\) là \(I\)
Hãy tìm công thức hóa học của chất X có khối lượng mol MX = 170 (g/mol), thành phần các nguyên tố theo khối lượng: 63,53% Ag; 8,23% N, còn lại O.
Gọi ông thức hóa học của X có dạng là AgxNyOz (x, y, z thuộc N)
%O = 100% − 63,53% − 8,23% = 28,24%
Ta có: nAg:nN:nO = 63,53/108 : 8,23/14 : 28,24/16
⇒ x:y:z = 0,588 : 0,588 : 1,765
⇒ x:y:z = 1:1:3
Vậy công thức hóa học của hợp chất X là AgNO3
Có: %O = 100 - 63,53 - 8,23 = 28,24%
Gọi CTHH cần tìm là AgxNyOz.
\(\Rightarrow x:y:z=\dfrac{63,53}{108}:\dfrac{8,23}{14}:\dfrac{28,24}{16}=1:1:3\)
→ X có CTHH dạng (AgNO3)n
\(\Rightarrow n=\dfrac{170}{108+14+16.3}=1\)
Vậy: X là AgNO3
Phân tích một oxit của lưu huỳnh người ta thấy cứ 2 phần khối lượng S thì có 3 phần khối lượng oxi. Xác định công thức của oxit lưu huỳnh?
Coi: mS = 2a (g) ⇒ mO = 3a (g)
\(\Rightarrow n_S=\dfrac{2a}{32}=\dfrac{a}{16}\left(mol\right)\)
\(n_O=\dfrac{3a}{16}\left(mol\right)\)
Gọi CTHH cần tìm là SxOy.
\(\Rightarrow x:y=\dfrac{a}{16}:\dfrac{3a}{16}=1:3\)
Vậy: CTHH cần tìm là SO3.
Gọi x, y lần lượt là số ml của S và O
Do tỉ lệ số mol của các chất chình là tỉ lệ giữa sô phân tử của nguyên tố cấu tạo nên chất
⇒ Công thức tổng quát SxOy
Theo đề bài, ta có: mS/mO = 2/3
=> 32x/16y = 2/3
=> 96/x = 32/y
=> x/y = 32/96 = 1/3
=> x = 1;
y = 3
=> Công thức hóa học: SO3