Làm chi tiết hộ mình mình chx hiểu lắm kq ấy

Làm chi tiết hộ mình mình chx hiểu lắm kq ấy

Câu 14: B
\(\left\{{}\begin{matrix}n_{HNO_3}=0,1.0,1=0,01\left(mol\right)\\n_{H_2SO_4}=0,4.0,05=0,02\left(mol\right)\end{matrix}\right.\)
=> \(\left[H^+\right]=\dfrac{0,01+0,02.2}{0,1+0,4}=10^{-1}M\)
=> pH = 1
Câu 15: C
\(\left\{{}\begin{matrix}n_{H_2SO_4}=0,1.0,1=0,01\left(mol\right)\\n_{NaOH}=0,3.0,15=0,045\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,02<----0,01
=> \(\left[OH^-\right]=\dfrac{0,045-0,02}{0,1+0,15}=10^{-1}M\)
=> \(\left[H^+\right]=\dfrac{10^{-14}}{10^{-1}}=10^{-13}M\)
=> pH = 13
Câu 14: B
Đổi: 100 ml = 0,1 lít
400 ml = 0,4 lít
mol HNO3 = 0,1 x 0,1 = 0,01 (mol)
HNO3 ------> H(+) + NO3(-)
0,01mol -----> 0,01mol
mol H2SO4 = 0,05 x 0,4 = 0,02 (mol)
H2SO4 ------> 2H(+) + SO4(2-)
0,02 --------->2 x 0,02
= 0,04mol
---> Tổng mol H(+) = 0,01 + 0,04 = 0,05
Tổng lít dung dịch = 0,1 + 0,4 = 0,5
----> [H(+)] = 0,05 : 0,5 = 0,1 (M) ----->
pH = -log(0,1) = 1
Câu 15: C
Đổi: 100ml = 0,1 lít
150 ml = 0,15 lít
mol H2SO4 = 0,1 x 0,1 = 0,01 (mol)
H2SO4 ------> 2H(+) + SO4(2-)
0,01 --------->2 x 0,01
= 0,02mol
mol NaOH = 0,3 x 0,15 = 0,045 (mol)
NaOH -----> Na(+) + OH(-)
0,045 ----------------> 0,045
---> OH(-) dư; H(+) hết
----> OH(-) dư = 0,045 - 0,02 = 0,025 (mol)
----> tổng lít dung dịch = 0,1 + 0,15 = 0,25
----> [OH(-)] = 0,025 : 0,25 = 0,1 (M)
----> pH của OH(-) = -log(0,1) = 1
----> pH của dung dịch = 14 - 1 = 13.
Bằng phương pháp hóa học hãy nhận biết các chất sau:
a) Rượu etylic, axit axetic, dầu ăn tan trong rượu etylic.
b) Khí metan, etilen, cacbon đioxit.
a)
-Dùng quỳ tím để nhận biết ra axit axetic.
-Hai chất lỏng còn lại cho vào ống nghiệm đựng nước, chất nào tan hoàn toàn tạo thành hỗn hợp đồng chất là rượu etylic, chất nào không tan nổi lên trên, hỗn hợp tách thành hai lớp riêng biệt là dầu ăn.
b)
lấy mẫu thử và đánh dấu
- cho dung dịch nước vôi trong ( Ca(OH)2) vào các mẫu thử
+ mẫu thử nào xuất hiên kết tủa trắng -> CO2
CO2 + Ca(OH)2 -> CaCO3 + H2O
+ mẫu thử nào khong hiện tượng -> CH4 và C2H4 (1)
- dẫn mẫu thử nhóm (1) qua dung dịch brom
+ mẫu thử nào làm mất màu dd -> C2H4
C2H4 + Br2 -> C2H4Br2
- còn lại là CH4
a) Cho các chất hoà vào nước:
- Tan hết: C2H5OH
Tan không hết: CH3COOH
- Không tan: dầu ăn
b)
Dẫn qua dd Ca(OH)2 dư:
- Có kết tủa trắng: CO2
CO2 + Ca(OH)2 ---> CaCO3 + H2O
- Không hiện tượng: C2H4. CH4 (1)
Dẫn (1) qua dd Br2 dư:
- Mất màu Br2: C2H4
C2H2 + 2Br2 ---> C2H4Br2
- Không hiện tượng: CH4
\(m_{Al}=\dfrac{22.49,1}{100}=10,8\left(g\right)\\ \rightarrow m_{Fe}=22-10,8=11,2\left(g\right)\\ \Rightarrow\left\{{}\begin{matrix}n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\end{matrix}\right.\)
\(n_{CuO}=\dfrac{72}{80}=0,9\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
0,2------------------------->0,2
2Al + 6HCl ---> 2AlCl3 + 3H2
0,4--------------------------->0,6
=> nH2 = 0,2 + 0,6 = 0,8 (mol) => VH2 = 0,8.22,4 = 17,92 (l)
PTHH: CuO + H2 --to--> Cu + H2O
LTL: 0,9 > 0,8 => CuO dư
Theo pthh: nCuO (pư) = nCu = nH2 = 0,8 (mol)
=> mchất rắn = (0,9 - 0,8).80 + 0,8.64 = 59,2 (g)
mAl=10,8g
=>n Al=0,4 mol
m Fe=11,2g
=>n Fe=0,2 mol
2Al+6HCl->2AlCl3+3H2
0,4-------------------------0,6 mol
FE+HCl->FeCl2+H2
0,2---------------------0,2
=>vH2=0,8.22,4=17,92l
H2+CuO-to->Cu+H2O
n CuO=0,9 mol
=>m cr=0,8.64+0,1.80=59,2g
trong các dịp lễ hội, Tùng thường thấy các trường thường thả bong bóng bay. Về nhà Tùng mua bong bóng dùng ống bơm xe đạp bơm khí vào, cột dây rồi tung lên để thả nhưng bong bóng không bay lên đc. Tùng thắc mắc tại sao vậy?
Em hãy giải thích cho bạn Tùng hiểu vì sao có bong bóng bay đc, có bong bóng lại không bay đc.
đó là do H2 nhẹ hơn trong kk nên khi bơm vào sẽ hay lên còn khi cho kk vào bóng thì trọng lg sẽ nnagwj hơn nên sẽ ko bay đc
CH3COOH+NaOH->CH3COONa+H2O
0,05----------------0,05----------0,05
n CH3COONa=0,05 mol
=>mCH3COOH=0,05.60=3g
=>m C2H5OH=4,3g
=>CM NaOH=\(\dfrac{0,05}{0,1}=0,5M\)
trộn 100ml dung dịch H2SO4 20%( d=1,14) với 400g dung dịch BaCl2 5,2%. Khối lượng chất kết tủa và chất trong dung dịch thu đc lần lượt là?
Giúp mik vs ạ!
Theo đề bài ta có :
nH2SO4=\(\dfrac{\left(100.1,14\right).20}{98.100}\).100≈0,23(mol)
nBaCl2=\(\dfrac{400.5,2}{100.208}\)=0,1(mol)
Ta có PTHH :
BaCl2+H2SO4−>BaSO4↓+2HCl
0,1mol.......0,1mol.............0,1mol.......0,2mol
Theo PTHH ta có : nBaCl2=\(\dfrac{0,1}{1}\)mol<nH2SO4=\(\dfrac{0,23}{1}\)mol
=> nH2SO4 dư ( tính theo nBaCl2)
a) Ta có : mBaSO4 = 0,1.233=23,3(g)
=>H2SO4 du, HCl
`BaCl_2 + H_2 SO_4 -> BaSO_4↓ + 2HCl`
`0,1` `0,1`
`m_[dd H_2 SO_4] = 1,14 . 100 = 114 (g)`
`=> n_[H_2 SO_4] = [ 20 / 100 . 114 ] / 98 = 0,2 (mol)`
`n_[BaCl_2] = [ [ 5,2 ] / 100 . 400 ] / 208 = 0,1 (mol)`
Ta có: `[ 0,2 ] / 1 > [ 0,1 ] / 1`
`=>BaCl_2` hết, `H_2 SO_4` dư
`=> m_[BaSO_4] = 0,1 . 233 = 23,3 (g)`
`**` Chất trong dung dich thu được là: `BaSO_4` và `H_2 SO_4` dư
Theo đề bài ta có :
nH2SO4=\(\dfrac{400.5,2}{100.208}\)=0,1(mol)
Ta có PTHH :
BaCl2+H2SO4−>BaSO4↓+2HCl
0,1mol.......0,1mol.............0,1mol.......0,2mol
Theo PTHH ta có : nBaCl2=\(\dfrac{0,23}{1}\)mol
=> nH2SO4 dư ( tính theo nBaCl2)
a) Ta có : mBaSO4 = 0,1.233=23,3(g)
b) Ta có :
C%H2SO4(dư)=\(\dfrac{\text{0,2.36,5}}{\text{100.1,14+400−23,3}}.100\)≈1,49%
Giải chi tiết hộ mình ạ

a) - Dẫn các bình trên qua dung dịch nước vôi trong, nếu nước vôi trong xuất hiện kết tủa thì đó là khí CO2 . Còn lại CH4 và C2H2 không hiện tượng.
PTHH: CO2 + Ca(OH)2 ==> CaCO3 ↓↓+ H2O
- Dẫn CH4, C2H2 qua dung dịch Brom, nếu dung dịch Brom mất màu thì đó là khí C2H2 . Còn lại CH4 không hiện tượng.
PTHH: C2H2 + 2Br2 ===> C2H2Br4
2.
trích mẫu thử các dung dịch và đánh số thứ tự
- Dùng một mẩu quỳ tím lần lượt cho vào 3 mẫu thử
Hiện tượng: Quỳ tím hóa đỏ => CH3COOH
Không có hiện tượng: C2H5OH và CH3COOC2H5
- Cho 1 mẩu Na vào 2 ống nghiệm
Hiện tượng: Na phản ứng mãnh liệt có khí thoát ra => C2H5OH
C2H5OH + Na --> C2H5ONa + 1/2H2
Không có hiện tượng => CH3COOC2H5
1) Dẫn qua dd Ca(OH)2 dư:
- Có kết tủa trắng: CO2
CO2 + Ca(OH)2 ---> CaCO3
- Không hiện tượng: C2H2. CH4 (1)
Dẫn (1) qua dd Br2 dư:
- Mất màu Br2: C2H2
C2H2 + 2Br2 ---> C2H2Br4
- Không hiện tượng: CH4
2) Cho thử QT:
- Hoá hồng: CH3COOH
- Hoá tím: C2H5OH, CH3COOC2H5 (1)
Cho (1) tác dụng với Na:
- Na tan dần, sủi bọt khí: C2H5OH
2C2H5OH + 2Na ---> 2C2H5ONa + H2
- Không hiện tượng: CH3COOC2H5
3) Cho thử dd I2:
- Hoá xanh: hồ tinh bột
- Không hiện tượng: C6H12O6, C12H22O11, C2H5OH (1)
Cho (1) tác dụng với Na:
- Na tan dần, sủi bọt khí: C2H5OH
2C2H5OH + 2Na ---> 2C2H5ONa + H2
- Không hiện tượng: C6H12O6, C12H22O11 (2)
Cho (2) tác dụng với dd AgNO3/NH3:
- Có kết tủa trắng bạc: C6H12O6
C6H12O6 + Ag2O --NH3--> C6H12O7 + 2Ag
- Không hiện tượng: C12H22O11
hoà tan hoàn toàn 6,75g Al vào 2 lít dung dịch HCl thu đc dung dịch AlCl3 và khí H2
a) viết PTHH xảy ra
b) tính thể tích khí hiđro sinh ra (đktc)
c) tính khối lượng AlCl3 tạo thành sau phản ứng
d) tính nồng độ mol dung dịch HCl tham gia phản ứng
(biết Al= 27, H= 1, Cl= 35,5)
n Al=0,25 mol
2Al + 6HCl → 2AlCl3 + 3H2
0,25---0,75------0,25------0,375 mol
=>VH2=0,375.22,4=8,4l
=>m AlCl3=0,25.133,5=33,375g
=>CM HCl=\(\dfrac{0,75}{2}\)=0,375M
: Tính khối lượng P2O5 cần cho vào 2 lít dung dịch H3PO4 1M để thu được dung dịch H3PO4 3M.
n H3PO4=2 mol
P2O5+3H2O->2H3PO4
2-----------------------4
muốn lên H3PO4 3M
=>n H3PO4 sau pu=6 mol
=>n H3PO4 thêm là 4 mol
=>m P2O5=2.142=284g
bài cúi rồi mn giúp em nhanh với ạ:<
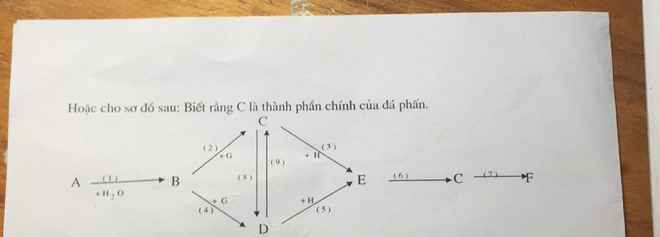
A: Ca
B: Ca(OH)2
C: CaCO3
D: Ca(HCO3)2
E: CO2
F: CaO
PTHH:
(1) Ca + 2H2O ---> Ca(OH)2 + H2
(2) Ca(OH)2 + CO2 ---> CaCO3
(3) Ca(OH)2 + 2CO2 ---> Ca(HCO3)2
(4) CaCO3 --to--> CaO + CO2
(5) Ca(HCO3)2 --to--> CaCO3 + CO2 + H2O
(6) CO2 + Ca(OH)2 ---> CaCO3 + H2O
(7) CaCO3 --to--> CaO + CO2
(8) CaCO3 + CO2 + H2O ---> Ca(HCO3)2
(9) Ca(HCO3)2 + Ca(OH)2 ---> 2CaCO3 + 2H2O
A: Ca
B: Ca(OH)2
C: CaCO3
D: Ca(HCO3)2
E: CaCl2
F: CaO
G: CO2
H: HCl
(1) Ca + 2H2O --> Ca(OH)2 + H2
(2) Ca(OH)2 + CO2 --> CaCO3 + H2O
(3) CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
(4) Ca(OH)2 + 2CO2 --> Ca(HCO3)2
(5) Ca(HCO3)2 + 2HCl --> CaCl2 + 2CO2 + 2H2O
(6) CaCl2 + Na2CO3 --> CaCO3 + 2NaCl
(7) CaCO3 --to--> CaO + CO2
(8) CaCO3 + CO2 + H2O --> Ca(HCO3)2
(9) Ca(HCO3)2 --to--> CaCO3 + CO2 + H2O