Hóa học
C2: A
C3: C
C4: C
C5: A
C6: A
C7: A
C8: C
C9: D
C10: B
Đúng 2
Bình luận (0)
Giúp mik vs mik đang cần gắp lắm
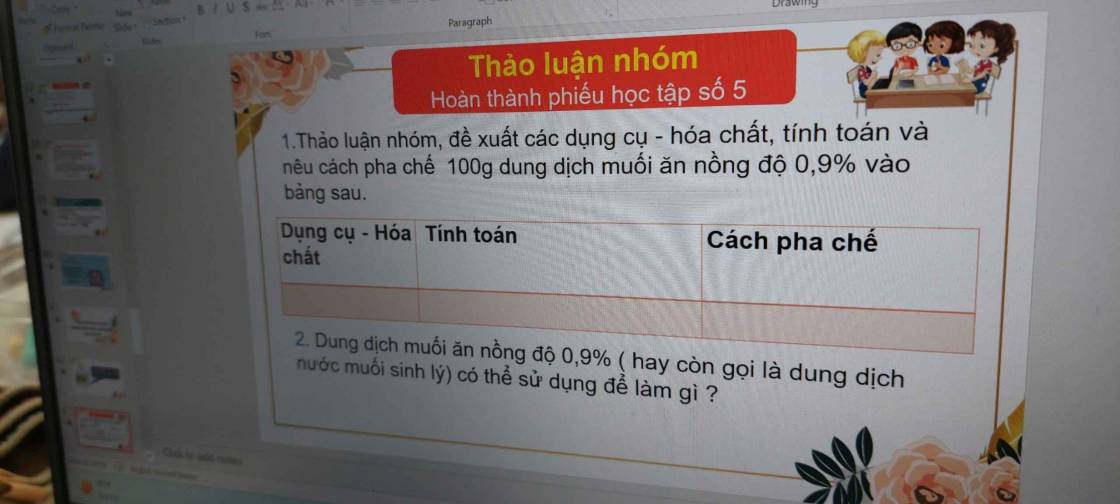
1. - Dụng cụ: Cân, cốc thủy tinh dung tích 250 ml, đũa thủy tinh, ống đong dung tích 100 ml.
Hóa chất: NaCl, nước cất.
- Tính toán: Ta có: \(m_{NaCl}=100.0,9\%=0,9\left(g\right)\)
⇒ mH2O = 100 - 0,9 = 99,1 (g)
- Cách pha chế:
+ Cân lấy 0,9 (g) NaCl cho vào cốc thủy tinh.
+ Đong 99,1 ml nước cất cho vào cốc thủy tinh, dùng đũa thủy tinh khuấy đều cho đến khi NaCl tan hoàn toàn.
2. Dung dịch NaCl 0,9% (nước muối sinh lý) dùng để:
+ Vệ sinh mắt, mũi, tai, họng, vết thương.
+ Truyền tĩnh mạch.
Đúng 2
Bình luận (0)
Tù muối magnessium sulfate MgSo4, nước cất và những dụng cụ cần thiết, hãy trình bày cách pha chế 250ml dung dịch Na2So4; 0,5M
cho dd chứa 48,5g CuCl2 tác dụng với dd chứa 24g NaOH
a, sau phản ứng chất nào dư và dư bnh
b, tính khối lượng kết tủa tạo thành
a, \(n_{CuCl_2}=\dfrac{48,5}{135}=\dfrac{97}{270}\left(mol\right)\)
\(n_{NaOH}=\dfrac{24}{40}=0,6\left(mol\right)\)
PT: \(CuCl_2+2NaOH\rightarrow2NaCl+Cu\left(OH\right)_2\)
Xét tỉ lệ: \(\dfrac{\dfrac{97}{270}}{1}>\dfrac{0,6}{2}\), ta được CuCl2 dư.
Theo PT: \(n_{CuCl_2\left(pư\right)}=n_{Cu\left(OH\right)_2}=\dfrac{1}{2}n_{NaOH}=0,3\left(mol\right)\)
\(\Rightarrow m_{CuCl_2\left(dư\right)}=48,5-0,3.135=8\left(g\right)\)
b, \(m_{Cu\left(OH\right)_2}=0,3.98=29,4\left(g\right)\)
Đúng 4
Bình luận (0)
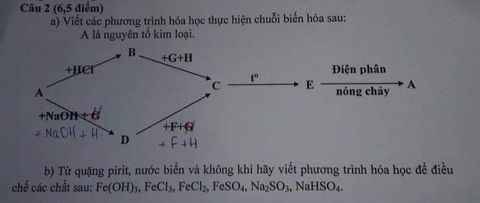
a, A là Al, B là AlCl3, C là Al(OH)3, D là NaAlO2, E là Al2O3, F là CO2, G là Na2CO3, H là H2O.
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
\(2AlCl_3+3Na_2CO_3+3H_2O\rightarrow2Al\left(OH\right)_3+3CO_2+6NaCl\)
\(2NaAlO_2+CO_2+3H_2O\rightarrow2Al\left(OH\right)_3+Na_2CO_3\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
\(Al_2O_3\underrightarrow{đpnc}2Al+\dfrac{3}{2}O_2\)
b, \(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
\(2NaCl+2H_2O\xrightarrow[cmn]{đpdd}2NaOH+Cl_2+H_2\)
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\) (Na2SO3)
\(H_2+Cl_2\underrightarrow{t^o}2HCl\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\) (FeCl3)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\) (Fe(OH)3)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\) (FeCl2)
\(SO_2+\dfrac{1}{2}O_2\underrightarrow{t^o}SO_3\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) (FeSO4)
\(NaOH+H_2SO_4\rightarrow NaHSO_4\) (NaHSO4)
Đúng 4
Bình luận (0)
Cho 15,4g hỗn hợp 2 kim loại Mg và Zn vào 500ml dung dịch HCl vừa đủ người ta thu được 6,72 lít khí (đktc).a, Viết các phương trình hoá học xảy rab,Tính phần trăm theo khối lượng của các chất rắn trong hỗn hợp ban đầu.c, Tính nồng độ mol/lít của dung dịch axit đã dùng.d, Cho hỗn hợp kim loại ở trên tác dụng với V (ml) dung dịch H2SO4 đặc 10% (DH2SO41,12g/ml).Xác định V?(Cho biết Mg24;Zn65;S32;O16;H1)(MÌNH CẦN GẤP!)
Đọc tiếp
Cho 15,4g hỗn hợp 2 kim loại Mg và Zn vào 500ml dung dịch HCl vừa đủ người ta thu được 6,72 lít khí (đktc).
a, Viết các phương trình hoá học xảy ra
b,Tính phần trăm theo khối lượng của các chất rắn trong hỗn hợp ban đầu.
c, Tính nồng độ mol/lít của dung dịch axit đã dùng.
d, Cho hỗn hợp kim loại ở trên tác dụng với V (ml) dung dịch H2SO4 đặc 10% (DH2SO4=1,12g/ml).Xác định V?
(Cho biết Mg=24;Zn=65;S=32;O=16;H=1)
(MÌNH CẦN GẤP!)
a) \(Mg+2HCl\rightarrow MgCl_2+H_2\) (1)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\) (2)
b) Gọi số mol của Mg là x còn số mol của Zn là y ta có:
\(24x+65y=15,4\) (*)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PTHH:
\(n_{H_2\left(1\right)}=n_{Mg}=x\)
\(n_{H_2\left(2\right)}=n_{Zn}=y\)
\(\Rightarrow x+y=0,3\) (**)
Từ (*) và (**) ta có hệ pt:
\(\left\{{}\begin{matrix}24x+65y=15,4\\x+y=0,3\end{matrix}\right.\)
Giải hệ ta có: \(\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%m_{Mg}=\dfrac{0,1\cdot24}{15,4}\approx16\%\)
\(\Rightarrow\%m_{Zn}=\dfrac{0,2\cdot65}{15,4}\approx84\%\)
c) Theo PTHH: \(n_{HCl\left(1\right)+\left(2\right)}=0,1\cdot2+0,2\cdot2=0,6\left(mol\right)\)
\(\Rightarrow C_{M,HCl}=\dfrac{0,6}{0,5}=1,2M\)
d) \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\) (3)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\) (4)
Ta có: \(\left\{{}\begin{matrix}n_{H_2SO_4\left(3\right)}=n_{Mg}=0,1\left(mol\right)\\n_{H_2SO_4\left(4\right)}=n_{Zn}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2SO_4}=0,1+0,2=0,3\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,3\cdot98=29,4\left(g\right)\)
\(\Rightarrow V_{H_2SO_4}=\dfrac{29,4}{1,12}=26,25\left(ml\right)\)
Đúng 1
Bình luận (3)
tính pH của dung dịch H2SO4 0,025M
Ta có: [H+] = 0,025.2 = 0,05 (M)
⇒ pH = -log[H+] ≃ 1,3
Đúng 2
Bình luận (0)
Một oxide có công thức x2o có tổng số hạt trong phân tử là 66 và số hạt mang điện nhiều hơn số không mang điện là 22 xác định công thức của oxit đó biết oxi gen n = p = e = 8
\(\Rightarrow X_2=66-24=42\)
\(\Rightarrow X=21\)
\(\Rightarrow2p_X+n_X=21\left(1\right)\)
\(4p_X+16-2n_X-8=22\)
\(\Leftrightarrow4p_X-2n_X=14\)
\(\Rightarrow2p_X-n_X=7\left(2\right)\)
Từ 1, 2 suy ra :
\(4p_X=28\)
\(\Rightarrow p_X=7\)
-> Nito (N)
-> N2O
Đúng 0
Bình luận (0)
Để trung hòa 300ml dung dịch X chứa NaOH 0,5 M và Ba(OH)2 aM cần 200 ml dung dịch hỗn hợp Y chứa HCl 1 M và H2SO4 0,5M ; sau phản ứng thu được m gam kết tủa. Tính giá trị a,m?
Ta có: \(n_{H^+}=n_{HCl}+2n_{H_2SO_4}=0,2.1+2.0,2.0,5=0,4\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
⇒ nOH- = nH+ = 0,4 (mol)
Mà: \(n_{OH^-}=n_{NaOH}+2n_{Ba\left(OH\right)_2}=0,3.0,5+2.0,3.a\left(mol\right)\)
⇒ 0,3.0,5 + 2.0,3.a = 0,4 ⇒ a = 5/12 (M)
\(n_{Ba^{2+}}=n_{Ba\left(OH\right)_2}=0,3.\dfrac{5}{12}=0,125\left(mol\right)\)
\(n_{SO_4^{2-}}=n_{H_2SO_4}=0,2.0,5=0,1\left(mol\right)\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
\(\Rightarrow n_{BaSO_4}=0,1\left(mol\right)\Rightarrow m=m_{BaSO_4}=0,1.233=23,3\left(g\right)\)
Đúng 2
Bình luận (0)