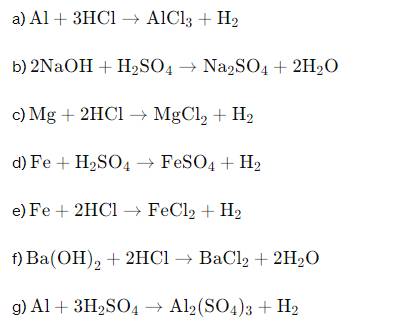Viết phương trình hoàn thành chuỗi phản ứng hóa học sau ghi rõ điều kiện nếu có : CO2 -> CaCO3 -> CaO -> CaSO4 -> CaCO3
Hóa học
1.CO2 + Ca(OH)2 -> CaCO3 + H2O (Phản ứng tạo kết tủa canxi cacbonat trong nước) 2.CaCO3 -> CaO + CO2 (Phản ứng phân hủy canxi cacbonat thành vôi sống và khí cacbonic) 3. CaO + H2SO4 -> CaSO4 + H2O (Phản ứng tạo kết tủa canxi sunfat trong nước)4.CaSO4 + Na2CO3 -> CaCO3 + Na2SO4 (Phản ứng trao đổi ion giữa canxi sunfat và natri cacbonat tạo ra kết tủa canxi cacbonat và natri sunfat)
Đúng 0
Bình luận (0)
c1 Hoàn thành các pthh sau
a) Al+? ----> Alcl+H2
b)NaoH+?---->Na2So4+H2o
C)Mg+Hcl---->? +H2
D) ?+H2so4---->Fecl2 +H2
e) ?+Hcl ---->Fecl2+H2
F) Ba(OH)2+?---->Bacl2+H2o
g) ? +H2So4---->al2(so4)3 =H2
a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
c, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
d, \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
e, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
f, \(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
g, \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Đúng 0
Bình luận (0)
1- Đốt cháy hoàn toàn 4,6 gam một hợp chất A cần dùng vừa đủ V lít khí Oxygen (ở 25°C, áp suất I bar). Sau phản ứng thu được 8,8 gam CO2 và 5,4 gam H,O.
a) Tinh V.
b) Tìm công thức phân tử của A biết tỉ khối của A so với Hydrogen là 23.
a, BTKL, có: mA + mO2 = mCO2 + mH2O
⇒ mO2 = 8,8 + 5,4 - 4,6 = 9,6 (g)
\(\Rightarrow n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,3.24,79=7,437\left(l\right)\)
b, \(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,2.12 + 0,6.1 = 3 (g) < mA
→ A gồm C, H và O.
⇒ mO = 4,6 - 3 = 1,6 (g)
\(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,2:0,6:0,1 = 2:6:1
→ A có dạng (C2H6O)n
Mà: MA = 23.2 = 46 (g/mol)
\(\Rightarrow n=\dfrac{46}{12.2+6.1+16.1}=1\)
Vậy: A là C2H6O.
Đúng 0
Bình luận (0)
- Viết phương trình điều chế oxide
- trình bày được mối quan hệ giữa acid, base, oxide và muối ; rút ra được kết luận về tính chất hoá học của acid,base,oxide
- trình bày khái niệm thang pH, các giá trị của thang pH
- Khái niệm , công thức tính nồng độ mol, nồng độ dung dịch
Cho 6,952g KMnO4 tác dụng với 1 lượng dư dung dịch HCl đặc, khí clo tạo thành được dẫn đi chậm qua ống đựng 7,8g kim loại A(hóa trị không đổi) nung nóng. Kết thúc phản ứng, chia chất rắn thu được thành 2 phần bằng nhau : Phần I: Tác dụng với lượng dư dung dịch axít HCl làm thoát ra 112ml khí H2(đktc).
phần II: khuấy kĩ trong dung dịch AgNO3 dư thu được m gam kết tủa.
xác định kim loại A và tính m. Biết các phản ứng xảy ra hoàn toàn.
Đọc tiếp
Cho 6,952g KMnO4 tác dụng với 1 lượng dư dung dịch HCl đặc, khí clo tạo thành được dẫn đi chậm qua ống đựng 7,8g kim loại A(hóa trị không đổi) nung nóng. Kết thúc phản ứng, chia chất rắn thu được thành 2 phần bằng nhau : Phần I: Tác dụng với lượng dư dung dịch axít HCl làm thoát ra 112ml khí H2(đktc). phần II: khuấy kĩ trong dung dịch AgNO3 dư thu được m gam kết tủa. xác định kim loại A và tính m. Biết các phản ứng xảy ra hoàn toàn.
Trình bày bằng lời và viết phương trình hóa học (nếu có) Bằng phương pháp hóa học hãy nhận biết: a) 4 dung dịch không màu:NaOH, Na2SO4, H2SO4, HCl. b) 4 dung dịch không màu:NaCl, Ba(OH)2, NaOH, Na2SO4 (chỉ dùng quỳ tím).
a, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: Na2SO4
+ Quỳ hóa đỏ: H2SO4, HCl (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: H2SO4
PT: \(BaCl_2+H_2SO_4\rightarrow BaSO_{4\downarrow}+2HCl\)
+ Không hiện tượng: HCl.
- Dán nhãn.
b, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: Ba(OH)2, NaOH (1)
+ Quỳ không đổi màu: NaCl, Na2SO4 (2)
- Cho mẫu thử nhóm (1) và (2) pư lần lượt với nhau.
+ Có tủa trắng: nhóm (1) là Ba(OH)2, nhóm (2) là Na2SO4
PT: \(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\)
+ Còn lại là NaOH ở nhóm (1) và NaCl ở nhóm (2)
- Dán nhãn.
Đúng 0
Bình luận (0)
Câu 1: Sản phẩm chính của phản ứng tách HBr của Ch3CH(CH3)CHBrCH3 là:A. 2-methylbut-2-en B. 3-methylbut-2-en C. 3-metyl-but-1-en D. 2-methylbut-1-enCâu 2: Khi phản ứng với CuO alcohol bậc 2 bị oxi hóa không hoàn toàn thànhA. Kentone B. Andehyde C. Carbon dioxide D. Carboxylic acidCâu 3: Acid Malonic có tổng số nguyên tử trong phân tử là:A.11 B.9 C.10 D. 12
Đọc tiếp
Câu 1: Sản phẩm chính của phản ứng tách HBr của Ch3CH(CH3)CHBrCH3 là:
A. 2-methylbut-2-en B. 3-methylbut-2-en C. 3-metyl-but-1-en D. 2-methylbut-1-en
Câu 2: Khi phản ứng với CuO alcohol bậc 2 bị oxi hóa không hoàn toàn thành
A. Kentone B. Andehyde C. Carbon dioxide D. Carboxylic acid
Câu 3: Acid Malonic có tổng số nguyên tử trong phân tử là:
A.11 B.9 C.10 D. 12
Khi cho một lượng dung dịch phenol trong etanol với Na(dư) thấy sinh ra 6,72l khí ở (đktc). Nếu cho cùng lượng dung dịch đó tác dụng với nước Brom dư hì tạo thành 16,55gam kết tủa trắng. Tính thành phần % theo khối lượng phenol có trong hỗn hợp ban đầu
Theo đề bài ta có hệ phương trình:
\(\left\{{}\begin{matrix}\dfrac{x}{y}+\dfrac{y}{2}=\dfrac{6,72}{22,4}=0,3\\331y=16,55\end{matrix}\right.\)
Giải ra ta được :
x = 0,55
y = 0,05
=> \(mC_2H_5OH=0,55.46=25,3\left(g\right)\)
=> \(mC_6H_5OH=0,05.94=4,7\left(g\right)\)
=> \(\%m_{C_2H_5OH}=\dfrac{25,3.100}{25,3+4,7}=84,33\%\)
=> \(\%m_{C_6H_5OH}=100-84,33=15,67\%\)
Đúng 4
Bình luận (2)
Người ta cho một lượng Zn vừa đủ tác dụng với 100g dd Hcl 7,3%, tính C% muối tạo thành
\(m_{HCl}=\dfrac{100\times7,3\%}{100\%}=7,3\left(g\right)\)
\(n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Mol (pt): 1 2 1 1
Mol (đề): 0,2
Theo pt, ta có: \(n_{ZnCl_2}=n_{Zn}=n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{0,2}{2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,1\cdot65=6,5\left(g\right)\\m_{H_2}=0,1\cdot2=0,2\left(g\right)\\m_{ZnCl_2}=0,1\cdot136=13,6\left(g\right)\end{matrix}\right.\)
Theo ĐLBTKL, ta có: \(m_{\text{dd }ZnCl_2}=m_{Zn}+m_{\text{dd }HCl}-m_{H_2}\)
\(=6,5+100-0,2=106,3\left(g\right)\)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{13,6}{106,3}\cdot100\%\approx12,79\%\)
Đúng 0
Bình luận (0)
Cần pha bao nhiêu gam dung dịch C2H5OH 8% vào 400 gam dung dịch C2H5OH 20% để được dung dịch C2H5OH 16%
Khối lượng rượu có trong 400g dd \(C_2H_5OH\) 20%
\(m_{C_2H_5OH}=\dfrac{400.20\%}{100\%}=80g\)
Khối lượng dd \(C_2H_5OH\) 8% cần thêm
\(C_{\%C_2H_5OH}=\dfrac{80+\dfrac{m_{C_2H_5OH.thêm}.8\%}{100\%}}{m_{C_2H_5OH.thêm}+400}\cdot100\%=16\%\\ \Rightarrow m_{C_2H_5OH.thêm}=200g\)
Đúng 1
Bình luận (3)