Hoà tan 10,2g Al2O3 vào trong dd có 7,3g HCl a. Sau pư có chất nào dư ko? Nếu còn khối lượng là bao nhiêu? b. Tính khối lượng muối tạo thành sau pư
Hóa học
\(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\\ pthh:Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ LTL:\dfrac{0,1}{2}>\dfrac{0,2}{6}\)
=> nhôm oxit dư
\(n_{Al_2O_3\left(p\text{ư}\right)}=\dfrac{1}{6}n_{HCl}=\dfrac{1}{30}\left(mol\right)\\ m_{Al\left(d\right)}=\left(0,1-\dfrac{1}{30}\right).102=6,8\left(g\right)\\ n_{AlCl_3}=\dfrac{1}{3}n_{HCl}=\dfrac{1}{15}\left(mol\right)\\ m_{AlCl_3}=\dfrac{1}{15}.133,5=8,9\left(g\right)\)
Đúng 3
Bình luận (1)
a. \(n_{Al_2O_3}=\dfrac{10.2}{102}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{7.3}{36,5}=0,2\left(mol\right)\)
PTHH : Al2O3 + 6HCl -> 2AlCl3 + 3H2O
\(\dfrac{0.2}{6}\) 0,2 \(\dfrac{0.4}{6}\)
Ta thấy : \(\dfrac{0.1}{1}>\dfrac{0.2}{6}\) => Al2O3 dư
\(m_{Al_2O_3\left(dư\right)}=\left(0,2-\dfrac{0.2}{6}\right).102=17\left(g\right)\)
b. \(m_{AlCl_3}=\dfrac{0.4}{6}.133,5=8,9\left(g\right)\)
a/
`n_(Al_2O_3) = (10,2)/)(27 . 2 + 16. 3) =0,1 mol`
`n_(HCl) = (7,3)/(1+ 35,5) = 0,2 mol`
PTHH :
`Al_2O_3 + 6HCl -> 2AlCl_3 + 3H_2O`
Nhận thấy : `(0,1)/1 > 0,2/6 -> Al_2O_3` dư và tính theo `HCl`
Ta có :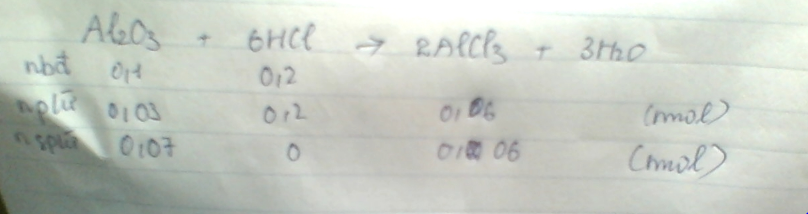
`m_(Al_2O_3)` dư `= 0,07 . 102 =7,14g`
`m_(AlCl_3)=0,06 .133,5 =8,01g`
Đúng 0
Bình luận (1)
Hoà tan hoàn toàn 33,3g hỗn hợp A gồm Na, Ca, Na2O, CaO vào 200,4g nước thu đc dung dịch B có 12g NaOH. Sục từ từ 21,28 lit CO2 (đktc) vào dd B thu đc kết tủa và dd C.
a) Tính khối lượng kết tủa
b) Tính nồng độ phần trăm các chất trong dd C
Hòa tan 25g cacl26h2o vào nước thu được 312ml dung dịch có khối lượng riêng 1.09 g/ml. TÍNH CM c% của dung dịch thu được
\(n_{CaCl_2.6H_2O}=\dfrac{25}{219}\left(mol\right)\)
=> \(n_{CaCl_2}=\dfrac{25}{219}\left(mol\right)\)
\(C_M=\dfrac{\dfrac{25}{219}}{0,312}=\dfrac{3125}{8541}M\)
\(m_{dd}=1,09.312=340,08\left(g\right)\)
\(C\%=\dfrac{\dfrac{25}{219}.111}{340,08}.100\%=3,726\%\)
Đúng 1
Bình luận (0)
Hấp thu hoàn toàn 34,4 g hỗn hợp khí X gồm CO2 và SO2 vào dung dịch chứa 1,4 mol KOH thu được dung dịch Y. Cho dung dịch thu được tác dụng với lượng dư dung dịch Ca(HCO3)2 thu đc 88 g kết tủa. Tỉ lệ số mol của CO2 với SO2 là bao nhiêu?
Đốt cháy 4,48 lít khí metan (CH4) trong bình chứa 13,44 lít khí Oxi. Sau khi phản ứng kết thúc thu được khí cacbonic và nước
a. Viết phương trình hóa học xảy ra
b. Chất nào còn dư sau phản ứng và dư bao nhiêu
c Tính thể tích khí cacbonic tạo thành sau phản ứng
\(n_{CH_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\
n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\
pthh:CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\\
LTL:\dfrac{0,2}{1}< \dfrac{0,6}{2}\)
=> Oxi dư
\(n_{O_2\left(p\text{ư}\right)}=2n_{CH_4}=0,4\left(mol\right)\\
m_{O_2\left(d\right)}=\left(0,6-0,4\right).32=6,4\left(g\right)\\
n_{CO_2}=n_{CH_4}=0,2\left(mol\right)\\
V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{CH_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\
n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\
pthh:CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\) '
\(LTL:\dfrac{0,4}{1}>\dfrac{0,6}{2}\)
=> CH4 dư
\(n_{CH_4\left(p\text{ư}\right)}=n_{CO_2}=\dfrac{1}{2}n_{O_2}=0,3\left(mol\right)\\
m_{CH_4\left(d\right)}=\left(0,4-0,3\right).16=1,6\left(g\right)\\
V_{CO_2}=0,3.22,4=6,72\left(l\right)\)
Đúng 0
Bình luận (2)
Hòa tan 10,8 g Al vào 300 ml dung dịch axit clohiđric HCl, sau phản ứng thu được muối nhôm clorua AlCl3 và khí hidro a. viết phương trình hóa học xảy ra b. tính thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn c. Tính khối lượng muối axit AlCl3 tạo thành d. Tính nồng độ mol của dung dịch HCl đã dùng e. tính nồng độ mol của dung dịch thu được sau phản ứng (coi thể tích dung dịch trước và sau phản ứng là không đổi)
Đọc tiếp
Hòa tan 10,8 g Al vào 300 ml dung dịch axit clohiđric HCl, sau phản ứng thu được muối nhôm clorua AlCl3 và khí hidro
a. viết phương trình hóa học xảy ra
b. tính thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn
c. Tính khối lượng muối axit AlCl3 tạo thành
d. Tính nồng độ mol của dung dịch HCl đã dùng
e. tính nồng độ mol của dung dịch thu được sau phản ứng (coi thể tích dung dịch trước và sau phản ứng là không đổi)
\(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\
pthh:2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,4 1,2 0,4 0,6
\(V_{H_2}=0,6.22,4=13,44\left(l\right)\\
m_{AlCl_3}=133,5.0,4=53,4\left(g\right)\\
C_{M\left(HCl\right)}=\dfrac{1,2}{0,3}=4M\\
C_{M\left(AlCl_3\right)}=\dfrac{0,4}{0,3}=1,3M\)
Đúng 4
Bình luận (2)
cho 27,4 g Kali tác dụng với 300 gam nước. sau phản ứng thu được dung dịch Bari Hiđroxit và khí hidro
a. viết phương trình hóa học xảy ra
b. tính thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn
c. Tính nồng độ phần trăm của dung dịch Bari Hiđroxit
nBa=\(\dfrac{27,4}{137}\)=0,2(mol)
pthh:Ba+2H2O→Ba(OH)2+H2↑
0,2 0,4 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\\ m_{\text{dd}}=27,4+300-\left(0,2.2\right)=327\left(g\right)\\ m_{Ba\left(OH\right)_2}=171.0,2=34,2\left(g\right)\\ C\%_{Ba\left(OH\right)_2}=\dfrac{34,2}{327}.100\%=10,5\%\)
Đúng 1
Bình luận (2)
cho 27,4 g Kali tác dụng với 300 gam nước. sau phản ứng thu được dung dịch Bari Hiđroxit và khí hidro
a. viết phương trình hóa học xảy ra
b. tính thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn
c. Tính nồng độ phần trăm của dung dịch Bari Hiđroxit
\(n_{Ba}=\dfrac{27,4}{137}=0,2\left(mol\right)\\ pthh:Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\)
0,2 0,4 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(L\right)\\
m_{\text{dd}}=27,4+300-\left(0,2.2\right)=327\left(g\right)\\
C\%_{Ba\left(OH\right)_2}=\dfrac{171.0,2}{327}.100\%=10,5\%\)
Đúng 3
Bình luận (0)
Hòa tan hết 30 gam hỗn hợp gồm một số kim loại trong dung dịch H2SO4 đặc, nóng (dư) thấy thoát ra 0,15 mol SO2; 0,1 mol S và 0,05 mol H2S. a) Tính số mol H2SO4 đã phản ứng. b) Tính khối lượng muối thu được sau phản ứng. (Giải bằng cách lớp 9 nhé!)
cách lớp 9 của bn là như thế nào ấy nhỉ :) ?
Đúng 5
Bình luận (3)
Cho V lít Ba(OH)2 2M pư với 100ml HCl 0,5M thu đc dung dịch A. Tính V và CM của dung dịch A.
\(n_{HCl}=0,1.0,5=0,05\left(mol\right)\)
PTHH: Ba(OH)2 + 2HCl --> BaCl2 + 2H2O
0,025<----0,05---->0,025
=> \(V=\dfrac{0,025}{2}=0,0125\left(l\right)\)
\(C_{M\left(A\right)}=\dfrac{0,025}{0,0125+0,1}=\dfrac{2}{9}M\)
Đúng 4
Bình luận (0)
100ml = 0,1 (l)
VHCl = 0,1 (l)
=> nHCl = CM.V = 0,1.0,5 = 0,05 (mol)
Ba(OH)2 + 2HCl -- > BaCl2 + 2H2O
0,025 0,05 0,025 0,05
VBa(OH)2 = n/CM = 0,025 / 2 = 0,0125 (l)
CMBaCl2 = n/V = 0,025 / 0,0125 = 2M
Đúng 1
Bình luận (0)


















