Mọi người giúp mình với
Cần dùng bao nhiêu ml dd H2SO4 2,5M và bao nhiêu ml dd H2SO4 1M để khi trộn với nhau được dd H2SO4 1,5M ?
Hóa học
Áp dụng sơ đồ đường chéo:
\(\dfrac{V_{dd.H_2SO_4.2,5M}}{V_{dd.H_2SO_4.1M}}=\dfrac{1,5-1}{2,5-1,5}=\dfrac{1}{2}\)
Vậy trộn 2 dd với tỉ lệ thể tích là 1 : 2 thì được dd có nồng độ 1,5M
Đúng 3
Bình luận (1)
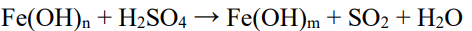
Cân bằng nhé
| \(Fe^{+n}-\left(m-n\right)e\rightarrow Fe^{+m}\) | \(\times2\) |
| \(S^{+6}-2e\rightarrow S^{+4}\) | \(\times\left(m-n\right)\) |
\(2Fe\left(OH\right)_n+\left(m-n\right)H_2SO_4\rightarrow2Fe\left(OH\right)_m+\left(m-n\right)SO_2+0H_2O\)
Đề đáng lẽ ra sản phẩm phải là \(Fe_2\left(SO_4\right)_3\) bạn nhỉ?
Đúng 1
Bình luận (0)
CaO dùng làm chất khử chua đất trồng là ứng dụng tính chất hóa học gì của CaO?
A. Tác dụng với axit. B. Tác dụng với bazơ.
C. Tác dụng với oxit axit. D. Tác dụng với muối.
Để khử chua đất, ta phải dùng chất có tính bazo :
$CaO + H_2O \to Ca(OH)_2$
CaO tan trong đất tạo Canxi hidroxit tác dụng với axit
Đáp án A
Đúng 3
Bình luận (0)
 câu c tính sao v ạ
câu c tính sao v ạ
thôi mình làm luôn cho
\(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
Đổi : VHCl = 200ml = 0,2 l
\(n_{HCl}=CM.V=2,5.0,2=0,5\left(mol\right)\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
0,25 0,5 0,25 0,25 (mol)
LTL : 0,3 / 1 > 0,5/2
muối là CuCl2
=> \(m_{CuCl_2}=0,25.135=33,75\left(g\right)\)
m rắn sau pứ là mCu dư lại
\(n_{Cu\left(dư\right)}=0,3-0,25=0,05\left(mol\right)\)
=> m rắn sau pứ = \(0,05.64=3,2\left(g\right)\)
dd sau pứ là CuCl2
\(CM_{CuCl_2}=\dfrac{n}{V}=\dfrac{0,25}{0,2}=1,25M\)
=> CuO dư , HCl đủ
Đúng 1
Bình luận (0)
câu c tính CM lấy V = 0,2 l đó bạn
lấy số mol rồi tính thôi
Đúng 0
Bình luận (0)
Cho 21,6g hỗn hợp 3 kim loại cu,zn,fe vào dung dịch h2so4 loãng dư ,phản ứng xong thu được 3g chất rắn ko tan và 6,72l khí (đktc)
A. Xác định thành phần phần trăm của mỗi kim loại có trong hỗn hợp
B. Xác định thành phần phần trăm của mỗi muối thu được trong hỗn hợp
A)
Chất rắn không tan là Cu
$\Rightarrow \%m_{Cu} = \dfrac{3}{21,6}.100\% = 13,8\%$
Gọi $n_{Zn} = a(mol) ; n_{Fe} = b(mol)$
$Zn + H_2SO_4 \to ZnSO_4 + H_2$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Ta có :
$n_{H_2} = a + b = 0,3(mol)$
$m_{hh} = 65a + 56b + 3 = 21,6(gam)$
Suy ra a = 0,2 ; b = 0,1
$\%m_{Zn} = \dfrac{0,2.65}{21,6}.100\% = 60,19\%$
$%m_{Fe} = \dfrac{0,1.56}{21,6}.100\% = 26,01\%$
b)
$m_{muối} = m_{ZnSO_4} + m_{FeSO_4} = 0,2.161 + 0,1.152 = 47,4(gam)$
$\%m_{ZnSO_4} = \dfrac{0,2.161}{47,4}.100\% = 67,93\%$
$\%m_{FeSO_4} = 100\% - 67,93\% = 32,07\%$
Đúng 3
Bình luận (0)
giúp bài nào cũng đc ạ
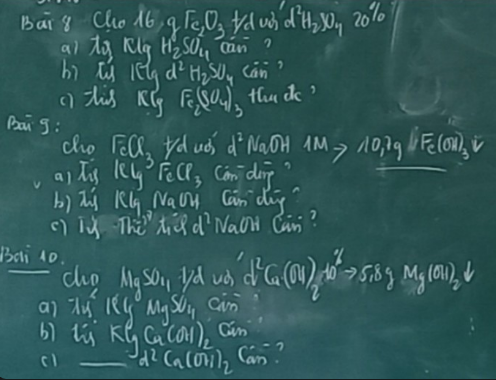
Bài 8 :
a) $n_{Fe_2O_3} = \dfrac{16}{160} = 0,1(mol)$
$Fe_2O_3 +3 H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O$
$n_{H_2SO_4} = 3n_{Fe_2O_3} = 0,1.3 = 0,3(mol)$
$m_{H_2SO_4} = 0,3.98 = 29,4(gam)$
b) $m_{dd\ H_2SO_4} = 29,4 : 20\% = 147(gam)$
c) $n_{Fe_2(SO_4)_3} = n_{Fe_2O_3} = 0,1(mol)$
$m_{Fe_2(SO_4)_3} = 0,1.400 = 40(gam)$
Đúng 4
Bình luận (0)
Bài 9 :
a) $n_{Fe(OH)_3} = \dfrac{10,7}{107} = 0,1(mol)$
$FeCl_3 + 3NaOH \to Fe(OH)_3 + 3NaCl$
$n_{FeCl_3} = n_{Fe(OH)_3} = 0,1(mol)$
$m_{FeCl_3} = 0,1.162,5= 16,25(gam)$
b) $n_{NaOH} = 0,1.3 = 0,3(mol)$
$m_{NaOH} = 0,3.40 = 12(gam)$
c) $V_{dd\ NaOH} = 0,1 : 1 = 0,1(lít)$
Đúng 4
Bình luận (0)
Bài 10 :
a) $n_{Mg(OH)_2} = \dfrac{5,8}{58} = 0,1(mol)$
\(MgSO_4+Ca\left(OH\right)_2\rightarrow Mg\left(OH\right)_2+CaSO_4\)
0,1 0,1 0,1 (mol)
$m_{MgSO_4} = 0,1.120 = 12(gam)$
b) $m_{Ca(OH)_2} = 0,1.74 = 7,4(gam)$
c) $m_{dd\ Ca(OH)_2} = 7,4 : 10\% = 74(gam)$
Đúng 4
Bình luận (0)
Xem thêm câu trả lời
có 4 lọ riêng biệt mất nhãn gồm :NH3 NO2 CO2 H2 trình bày phương pháp hóa học nhận biết các khí riêng biệt trên
- Đánh STT cho các lọ chứa khí
- Cho mẩu quỳ tím ẩm vào các lọ chứa khí, nếu thấy:
+ Quỳ tím hoá xanh: NH3
\(NH_3+H_2O⇌NH_4OH\)
+ Quỳ tím hoá đỏ: NO2.
\(4NO_2+O_2+2H_2O\rightarrow4HNO_3\)
+ Quỳ tím hoá hồng: CO2.
\(CO_2+H_2O⇌H_2CO_3\)
+ Quỳ tím không đổi màu: H2
Đánh STT cho các lọ chứa khí
Đúng 4
Bình luận (0)
Khí có màu nâu đỏ là NO2
Dùng quỳ tím ẩm:
+ quỳ tím ẩm chuyển sang màu xanh : NH3
+ quỳ tím ẩm chuyển sang màu hơi đỏ : CO2
+ quỳ tím ẩm không đổi màu : H2
Đúng 1
Bình luận (0)
Cho 11,1g hỗn hợp :Na va Zn t/d với dd HCl thu đc 4,48l H2(đktc)
a.Tính kl mỗi kim loại
bTính mHCl (phản ứng)
Gọi số mol của Na và Zn lần lượt là x và y
PTHH :
\(2Na+2HCl\rightarrow2NaCl+H_2\)
x -------- > x --------> x ----> 0,5x (mol)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
y-----> 2y -----> y ----> y (mol)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Ta có hệ pt:
23x + 65y = 11,1
0,5x + y = 0,2
giải hệ:
ta được :
x = 0,2
y = 0,1
mNa = 23x = 23.0,2 = 4,6(g)
mZn = 65y = 65.0,1 = 6,5 (g)
nHCl = x + 2y = 0,2 + 2.0,1 = 0,4(mol)
=> mHCl = 0,4.36,5 = 14,6(g)
Đúng 2
Bình luận (0)
a) CTHH: SX3
\(PTK_{SX_3}=40.2=80\left(đvC\right)\)
=> \(NTK_X=16\left(đvC\right)\)
=> X là Oxi (O)
b)
- SO3 được tạo ra từ nguyên tố S và O
- Trong 1 phân tử SO3 có 1 nguyên tử S và 3 nguyên tử O
- PTK của SO3 là 80 đvC
Đúng 2
Bình luận (0)
Hấp thụ hoàn toàn 6,72 lít CO2(đktc) vào 200ml dung dịch hỗn hợp NaOH aM và Ca(OH)2 bM thu được 8g kết tủa và dung dịch X chỉ chứa 21,12g muối. Tính giá trị của a, b
a)
\(\left\{{}\begin{matrix}n_{NaOH}=0,2a\left(mol\right)\\n_{Ca\left(OH\right)_2}=0,2b\left(mol\right)\end{matrix}\right.\); \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{8}{100}=0,08\left(mol\right)\)
TH1: Kết tủa không bị hòa tan
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,08<----0,08<------0,08
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
2x<--------x--------->x
\(Na_2CO_3+CO_2+H_2O\rightarrow2NaHCO_3\)
y<----------y------------------>2y
=> x + y + 0,08 = 0,3
=> x + y = 0,22 (1)
dd chứa 2 muối là \(\left\{{}\begin{matrix}Na_2CO_3:x-y\left(mol\right)\\NaHCO_3:2y\left(mol\right)\end{matrix}\right.\)
=> 106(x-y) + 84.2y = 21,12
=> 106x + 62y = 21,12 (2)
(1)(2) => x = 0,17 (mol); y = 0,05 (mol)
Ta có: \(n_{Ca\left(OH\right)_2}=0,2b=0,08\left(mol\right)\) => b = 0,4
Ta có: \(n_{NaOH}=0,2a=0,34\left(mol\right)\) => a = 1,7
TH2: Kết tủa bị tan 1 phần
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,2b----->0,2b----->0,2b
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
0,2a--->0,1a----->0,1a
\(Na_2CO_3+CO_2+H_2O\rightarrow2NaHCO_3\)
0,1a--->0,1a---------------->0,2a
\(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
u-------->u--------------->u
Ta có: \(n_{CaCO_3}=0,2b-u=0,08\) (*)
\(n_{CO_2}=0,2a+0,2b+u=0,3\) (**)
dd sau pư chứa \(\left\{{}\begin{matrix}NaHCO_3:0,2a\left(mol\right)\\Ca\left(HCO_3\right)_2:u\left(mol\right)\end{matrix}\right.\)
=> 84.0,2a + 162u = 21,12
=> 16,8a + 162u = 21,12 (***)
(*)(**)(***) => a = 5,5; b = -1,8; u = -0,44 (Vô lí)
Đúng 3
Bình luận (0)




















