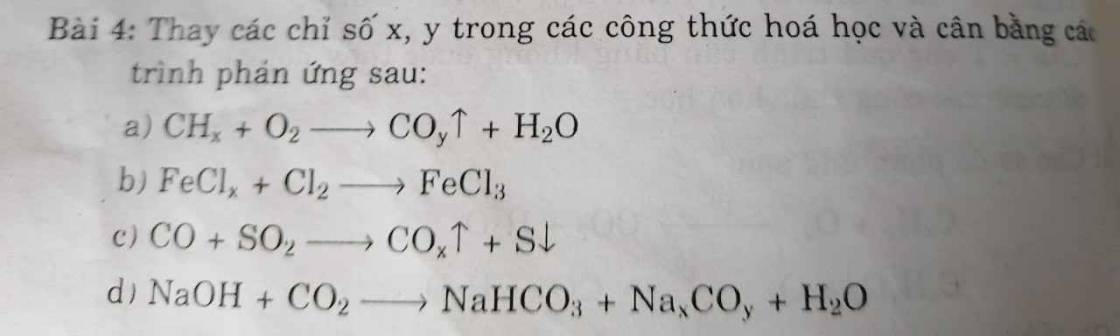Hóa học
Bài 8 :
$n_{Ca(OH)_2} = 0,4.1,5 = 0,6(mol)$
$2CO_2 + Ca(OH)_2 \to Ca(HCO_3)_2$
Theo PTHH :
$n_{Ca(HCO_3)_2} = 0,6(mol) \Rightarrow m = 0,6.162 = 97,2(gam)$
$n_{CO_2} = 0,6.2 = 1,2(mol) \Rightarrow V = 1,2.22,4 = 26,88(lít)$
Bài 9 :
$n_{Ba(OH)_2} = \dfrac{300.17,1\%}{171} = 0,3(mol)$
$SO_2 + Ba(OH)_2 \to BaSO_3 + H_2O$
Theo PTHH : $n_{SO_2} = n_{BaSO_3} = n_{Ba(OH)_2} =0,3(mol)$
$V = 0,3.22,4 = 6,72(lít)$
$a = 0,3.217= 65,1(gam)$
Bài 10 :
$CO_2 + Ba(OH)_2 \to BaCO_3 + H_2O$
Theo PTHH : $n_{CO_2} =n_{Ba(OH)_2} = n_{BaCO_3} = \dfrac{29,55}{197} = 0,15(mol)$
$V = 0,15.22,4 = 3,36(lít)$
$a = \dfrac{0,15}{1,5} = 0,1(lít) = 100(ml)$
Đúng 1
Bình luận (3)
Bài 5 :
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
Theo PTHH : $n_{CaCO_3} = n_{Ca(OH)_2} = n_{CO_2} = \dfrac{7,84}{22,4} = 0,35(mol)$
$m = 0,35.100 = 35(gam)$
$V = \dfrac{0,35}{2} = 0,175(lít)$
Bài 6 : $n_{Ba(HCO_3)_2} = \dfrac{25,9}{259} = 0,1(mol)$
$2CO_2 + Ba(OH)_2 \to Ba(HCO_3)_2$
$n_{Ba(OH)_2} = 0,1(moL) \Rightarrow x = \dfrac{0,1}{0,2} = 0,5M$
$n_{CO_2} = 0,2(mol) \Rightarrow V = 0,2.22,4 = 4,48(lít)$
Đúng 1
Bình luận (0)
Axit axectic có công thức cấu tạo là \(CH_3COOH\:\). Số nguyên tử H có trong hợp chất là bao nhiêu?Tại sao?
Công thức phân tử : $C_2H_4O_2$
Số nguyên tử Hidro : 4
Đúng 1
Bình luận (0)
Nung 16,2 gam hỗn hợp A gồm các oxit MgO, AL2O3; và MO trong một ống sứ rồi cho luồng khí H2 đi qua. Ở điều kiện thí nghiệm H2 chỉ khử MO với hiệu suất 80%. Lượng hơi nước tạo ra chỉ được hấp thụ 90% vào 15,3 gam dung dịch H2SO4, 90%, kết quả thu được dung dịch H2SO4 86,34%. Chất rắn còn lại trong ống được hòa tan trong một lượng vừa đủ axit HCl, thu được dung dịch B và còn lại 2,56 gam chất rắn kim loại M không tan. Lấy 1/10 dung dịch B cho tác dụng với dung dịch NaOH dư, lọc lấy kết tủa nung ở...
Đọc tiếp
Nung 16,2 gam hỗn hợp A gồm các oxit MgO, AL2O3; và MO trong một ống sứ rồi cho luồng khí H2 đi qua. Ở điều kiện thí nghiệm H2 chỉ khử MO với hiệu suất 80%. Lượng hơi nước tạo ra chỉ được hấp thụ 90% vào 15,3 gam dung dịch H2SO4, 90%, kết quả thu được dung dịch H2SO4 86,34%. Chất rắn còn lại trong ống được hòa tan trong một lượng vừa đủ axit HCl, thu được dung dịch B và còn lại 2,56 gam chất rắn kim loại M không tan. Lấy 1/10 dung dịch B cho tác dụng với dung dịch NaOH dư, lọc lấy kết tủa nung ở nhiệt độ cao đến khối lượng không đối thì thu được 0,28 gam oxit. a. Xác định kim loại M b. Tính % khối lượng các chất trong hỗn hợp A.
a)
$m_{H_2SO_4} = 15,3.90\% = 13,77(gam)$
Gọi $a_{H_2O} = a(mol) ; n_{H_2O\ hấp\ thụ} = a.90\% = 0,9a(mol)$
Ta có : $C\%_{H_2SO_4} = \dfrac{13,77}{0,9a.18 + 15,3}.100\% = 86,34\%$
$\Rightarrow a = 0,04$
$MO + H_2 \xrightarrow{t^o} M + H_2O$
Theo PTHH : $n_M = n_{H_2O} = 0,04(mol)$
$\Rightarrow M = \dfrac{2,56}{0,04} = 64(Cu)$
b) $n_{CuO\ pư} = n_{H_2O} = 0,04(mol)$
$n_{CuO\ ban\ đầu} = 0,04 : 80\% = 0,05(mol)$
$n_{MgO} = \dfrac{0,28}{40} = 0,007(mol)$
$\Rightarrow n_{MgO\ trong\ A} = 0,007.10 = 0,07(mol)$
$\%m_{CuO} = \dfrac{0,05.80}{16,2}.100\% = 24,7\%$
$\%m_{MgO} = \dfrac{0,07.40}{16,2}.100\% = 17,3\%$
$\%m_{Al_2O_3} = 100\% - 24,7\% - 17,3\% = 58\%$
Đúng 1
Bình luận (0)
Giúp em bài 3 với
Câu 3:
a) \(2Al\left(OH\right)_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+6H_2O\)
b) \(CuO+2HNO_3\rightarrow Cu\left(NO_3\right)_2+H_2O\)
c) \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
d) \(BaCO_3+2HCl\rightarrow BaCl_2+CO_2+H_2O\)
Đúng 1
Bình luận (0)
\(a) 2Al(OH)_3 + 3H_2SO_4 \to Al_2(SO_4)_3 + 6H_2O\\ b) CuO +2 HNO_3 \to Cu(NO_3)_2 +H_2O\\ c) 2NaOH + CO_2 \to Na_2CO_3 + H_2O\\ d)BaCO_3 + 2HCl \to BaCl_2 + CO_2 + H_2O\)
Đúng 1
Bình luận (0)
Mọi người cho mình hỏi \(I_2\) là đơn chất hay hợp chất ạ??Tại sao??
$I_2$ là đơn chất vì chỉ được cấu tạo từ một nguyên tố hóa học (nguyên tố Iot)
Đúng 1
Bình luận (0)
Hỗn hợp X gồm SO, và O, có tỉ khối so với H2 bằng 24. Đun nóng hỗn hợp X với xúc tác V.O, sau một thời gian thu được hỗn hợp Y, tỉ khối của Y so với X bằng 1,25. Tính hiệu suất phản ứng.
\(\overline{M}_X=24.2=48\left(g/mol\right)\)
Áp dụng sơ đồ đường chéo, ta có:
\(\dfrac{n_{SO_2}}{n_{O_2}}=\dfrac{48-32}{64-48}=\dfrac{1}{1}\)
Đặt \(n_{SO_2}=n_{O_2}=1\left(mol\right)\)
Gọi \(n_{SO_2\left(pư\right)}=a\left(mol\right)\)
PTHH: \(2SO_2+O_2\xrightarrow[V_2O_5]{t^o}2SO_3\)
ban đầu 1 1
phản ứng a----->0,5a
sau pư (1-a) (1-0,5a) a
=> \(n_Y=1-a+1-0,5a+a=2-0,5a\left(mol\right)\)
Theo ĐLBTKL: \(m_Y=m_X=32+64=96\left(g\right)\)
=> \(\overline{M}_Y=\dfrac{96}{2-0,5a}=1,25.48=60\left(g/mol\right)\)
=> a = 0,8 (mol)
Xét \(\dfrac{n_{SO_2}}{2}< \dfrac{n_{O_2}}{1}\left(\dfrac{1}{2}< \dfrac{1}{1}\right)\) => Hiệu suất phản ứng tính theo SO2
=> \(H=\dfrac{0,8}{1}.100\%=80\%\)
Đúng 2
Bình luận (0)
Tìm công thức hóa học của khí \(M_xO_y\), biết khí đó nặng hơn khí \(H_2\) 32 lần
Ta có : $PTK = xM + 16y = M_{H_2}.32 = 32.2 = 64(đvC)$
$\Rightarrow M = \dfrac{64 -16y}{x}$
| x | y | M |
| 1 | 1 | 48(loại) |
| 1 | 2 | 32(Lưu huỳnh) |
| 1 | 3 | 16(loại) |
| 2 | 3 | 8(loại) |
Vậy CTHH của khí cần tìm là $SO_2$
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 14,4 gam FeO trong dung dịch H,SO4 20% vừa đủ thu được dung dịch X. Hạ nhiệt độ của dung dịch X xuống 10°C thì thu được bao nhiêu gam FeSO4.10HO? Biết độ tan của FeSO4 ở 10°C là 15,6.
$FeO + H_2SO_4 \to FeSO_4 + H_2O$
$n_{FeSO_4} = n_{H_2SO_4} = n_{FeO} = \dfrac{14,4}{72} = 0,2(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,2.98}{20\%} = 98(gam)$
Sau phản ứng, $m_{dd} = 14,4 + 98 = 112,4(gam)$
Gọi $n_{FeSO_4.10H_2O} = a(mol)$
Sau khi tách tinh thể :
$n_{FeSO_4} = 0,2 -a(mol)$
$m_{dd} = 112,4 - 332a(gam)$
Ta có :
$C\%_{FeSO_4} = \dfrac{152(0,2-a)}{112,4 - 332a}.100\% = \dfrac{15,6}{15,6+100}$
$\Rightarrow a = 0,142(mol)$
$m_{FeSO_4.10H_2O} = 332.0,142 = 47,144(gam)$
Đúng 1
Bình luận (0)
a) \(x=4,y=2\)
\(\Rightarrow CH_4+2O_2\text{ }^{\underrightarrow{t^o}}CO_2+2H_2O\)
b) \(x=2\)
\(\Rightarrow2FeCl_2+Cl_2\text{ }^{\underrightarrow{t^o}}2FeCl_3\)
c) \(x=2\)
\(\Rightarrow2CO+SO_2\rightarrow2CO_2\uparrow+S\downarrow\)
d) \(x=2,y=3\)
\(\Rightarrow4NaOH+3CO_2\rightarrow2NaHCO_3+Na_2CO_3+H_2O\)
Đúng 1
Bình luận (0)
a) $CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
b) $2FeCl_2 + Cl_2 \to 2FeCl_3$
c) $2CO + 2SO_2 \xrightarrow{t^o} 3CO_2 + 2S$
d) $3NaOH + 2CO_2 \to NaHCO_3 + Na_2CO_3 + H_2O$
Đúng 0
Bình luận (0)