Cho 21,6g nhôm tác dụng vừa đủ với 300g đ H2SO4 loãng :
a ) Tính V H2 ở đhtc,
b) Tính c% H2SO4 ,
c) Tính C% muối sau phản ứng
Hóa học
a) $n_{Al} = \dfrac{21,6}{27} = 0,8(mol)$
$2Al +3 H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
Theo PTHH, $n_{H_2} = \dfrac{3}{2}n_{Al}= 1,2(mol)$
$V_{H_2} = 1,2.22,4 = 26,88(lít)$
b) $n_{H_2SO_4} = n_{H_2} = 1,2(mol)$
$C\%_{H_2SO_4} = \dfrac{1,2.98}{300}.100\% = 39,2\%$
c) Sau phản ứng, $m_{dd} = m_{Al} + m_{dd\ H_2SO_4} - m_{H_2} $
$= 21,6 + 300 - 1,2.2 = 319,2(gam)$
$n_{Al_2(SO_4)_3} = 0,4(mol)$
$C\%_{Al_2(SO_4)_3} = \dfrac{0,4.342}{319,2}.100\% = 42,86\%$
Đúng 2
Bình luận (0)
1.Nung nóng 14,7 (g) Bazơ của kim loại có hóa trị II đến khối lượng không đổi thu được 12 g 1 Oxit. Xác định CTHH của Bazơ.
2. Cho 200ml dd H2SO4 1M tác dụng 200g dd NaOH
a. Tính nH2SO4 , nNaOH
b. Dung dịch sau phản ứng làm quỳ tím chuyển màu gì?
c. Tính mNa2SO4.
1) Gọi CTHH của bazo là $R(OH)_2$
$R(OH)_2 \xrightarrow{t^o} RO + H_2O$
Theo PTHH :
$n_{RO} = n_{R(OH)_2} \Rightarrow \dfrac{12}{R + 16} = \dfrac{14,7}{R + 34}$
$\Rightarrow R = 64(Cu)$
Vậy CTHH bazo là $Cu(OH)_2$
2)
a) $n_{H_2SO_4} = 0,1.2 = 0,2(mol)$
$2NaOH + H_2SO_4 \to Na_2SO_4 +2 H_2O$
$n_{NaOH} = 2n_{H_2SO_4} = 0,4(mol)$
b) Dung dịch sau phản ứng không làm quỳ tím chuyển màu
c) $n_{Na_2SO_4} = n_{H_2SO_4] = 0,2(mol)$
$m_{Na_2SO_4} = 0,2.14 2= 28,4(gam)$
Đúng 1
Bình luận (0)
Cho 4,06 g hh Al và Zn td với 200ml dd HCl 2,3M.
a. Nếu pứ xảy ra hoàn toàn kl có tan hết ko?
b. Nếu thoát ra 2,128 l H2 thì mmuối là bao nhiêu?
(Giải cách dễ hiểu kiểu lớp 8 giúp em ạ, em cảm ơn ạ)
a) $n_{HCl} = 0,2.2,3 = 0,46(mol)$
Giả sử hh chỉ gồm $Al$ : $n_{Al} = \dfrac{4,06}{27} = 0,15(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
Ta thấy :
$n_{Al} : 2 < n_{HCl} : 6$ nên HCl dư $(1)$
Giả sử hh chỉ gồm $Mg : n_{Mg} = \dfrac{4,06}{24} = 0,17(mol)$
$Mg + 2HCl \to MgCl_2 + H_2$
Ta thấy :
$n_{Mg} :1 < n_{HCl} :2$ nên HCl dư $(2)$
Từ (1)(2) suy ra $HCl$ dư, kim loại tan hết
b) $n_{H_2} = \dfrac{2,128}{22,4} = 0,095(mol)$
Theo PTHH, $n_{HCl\ pư} = 2n_{H_2} = 0,19(mol)$
$m_{muối} = m_{hh} + m_{HCl} - m_{H_2} = 4,06 + 0,19.36,5 - 0,095.2 = 10,805(gam)$
Đúng 2
Bình luận (1)
Làm hộ mik 5 câu này với ạ mik đang cần gấp
\(5.MgO+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+2H_2O\\ MgCO_3+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O\\ n_{CO_2}=0,15\left(mol\right)\\ n_{MgCO_3}=n_{CO_2}=0,15\left(mol\right)\\ \Rightarrow\%m_{MgCO_3}=\dfrac{0,15.84}{20,6}.100=61,17\%\\ \%m_{MgO}=100-61,17=38,83\%\)
Đúng 1
Bình luận (0)
a) $Mg + 2HCl \to MgCl_2 + H_2$
b) Tỉ lệ số nguyên tử $Mg$ : số phân tử $HCl$ là $1 : 2$
Tỉ lệ số nguyên tử $Mg$ : số phân tử $MgCl_2$ là $1 : 1$
Tỉ lệ số nguyên tử $Mg$ : số phân tử $H_2$ là $1 : 1$
Đúng 3
Bình luận (0)
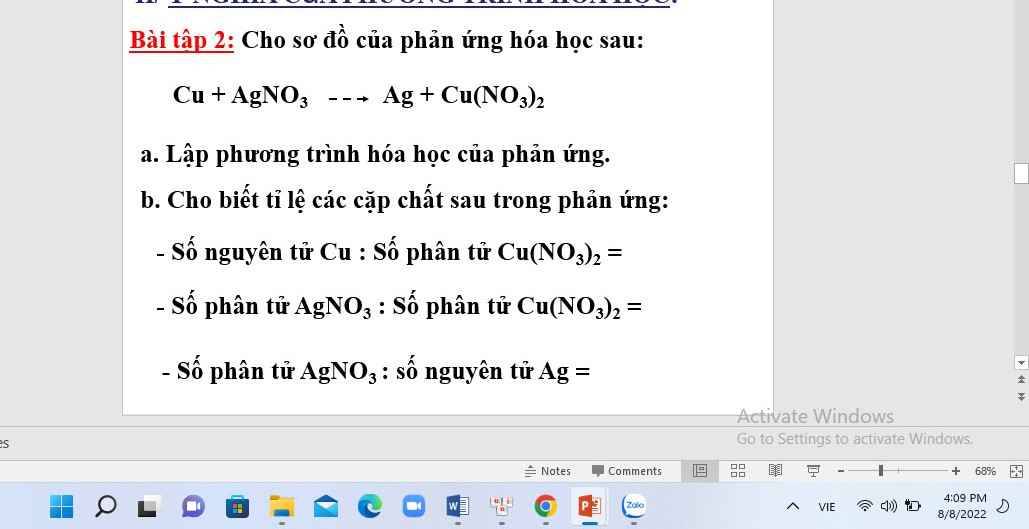
a: \(Cu+2AgNO_3\rightarrow2Ag+Cu\left(NO_3\right)_2\)
b: Số nguyên tử Cu:Số phân tử Cu(NO3)2: 1:1
Số phân tử AgNo3 và Số phân tử Cu(NO3)2: 1:2
Đúng 1
Bình luận (0)
hãy nêu các phương pháp chính để điều chế axit sunfuric đặc nêu vd
Nung nóng quặng pirit sắt ở nhiệt độ cao :
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
Oxi hóa $SO_2$ bằng $O_2$ ở nhiệt độ cao có mặt chất xúc tác :
$2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
Thu lấy sản phẩm, cho vào nước ta được axit sunfuric
$SO_3 + H_2O \to H_2SO_4$
Đúng 3
Bình luận (0)
Tham khảo:
Bước 1: Trước tiên, cần đốt cháy quặng firit sắt: 4FeS2 + 11O2 → 8SO2 + 2Fe2O3.
Bước 2: Sau đó oxi hóa SO2 bằng oxi trong điều kiện 400 đến 5000C, chất xúc tác V2O5: 2SO2 + O2 → 8SO3.
Bước 3: Axit sunfuric đặc hấp thụ SO3 tạo thành oleum với công thức tổng quát là H2SO4.nSO3: nSO3 + H2SO4 → H2SO4 .nSO3.
Bước 4: Pha loãng oleum thành axit sunfuric H2SO4 bằng lượng nước thích hợp: H2SO4 .nSO3 + (n+1) H2O→ (n+1)H2SO4.
Đúng 1
Bình luận (0)
Có một lọ đựng dd phenolphtalein (C20H14O4) và 4 ống nghiệm đánh số từ 1 đến 4 chứa một trong các dd loãng: HCl, NaCl, AlCl3, NaOH.Nhỏ vài giọt phenolphtalein vào cả 4 ống nghiệm. Ta thấy dd trong ống nghiệm 3 chuyển thành màu hồng. Sau đó, nhỏ vài giọt dd màu hồng này vào trong 3 ống nghiệm còn lại. Ta thấy dd trong ống nghiệm 1 chuyển thành màu hồng còn ống nghiệm 2 và 4 không màu.Xác định chất ban đầu trong ống nghiệm 1 và 3.
Đọc tiếp
Có một lọ đựng dd phenolphtalein (C20H14O4) và 4 ống nghiệm đánh số từ 1 đến 4 chứa một trong các dd loãng: HCl, NaCl, AlCl3, NaOH.
Nhỏ vài giọt phenolphtalein vào cả 4 ống nghiệm. Ta thấy dd trong ống nghiệm 3 chuyển thành màu hồng. Sau đó, nhỏ vài giọt dd màu hồng này vào trong 3 ống nghiệm còn lại. Ta thấy dd trong ống nghiệm 1 chuyển thành màu hồng còn ống nghiệm 2 và 4 không màu.
Xác định chất ban đầu trong ống nghiệm 1 và 3.
Ống nghiệm 3 chuyển màu hồng => Ống 3 là NaOH do NaOH làm phenolphtalein hóa hồng
Sau đó, nhỏ vài giọt dd màu hồng này vào trong 3 ống nghiệm còn lại. Ta thấy dd trong ống nghiệm 1 chuyển thành màu hồng => Ống 1 là NaCl do NaOH không phản ứng với NaCl
Ống nghiệm 2 và 4 không màu => Ống 2,4 tác dụng với phenolphtalein => Ống 2, 4 là HCl và AlCl3
Đúng 1
Bình luận (0)
Xin cách giải phương trình ạ
Đọc tiếp
Xin cách giải phương trình ạ
\(\left\{{}\begin{matrix}0,2x\left(56-M_M\right)=3,2\\0,4x\left(64-M_M\right)=8\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}11,2x-0,2xM_M=3,2\\25,6x-0,4xM_M=8\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}22,4x-0,4xM_M=6,4\\25,6x-0,4xM_M=8\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3,2x=1,6\\11,2x-0,2xM_M=3,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,5\\M_M=24\end{matrix}\right.\)
Đúng 1
Bình luận (0)
nếu 1 mol H2SO4 hấp thụ 1 mol SO3 thì thu đc oleum có công thức như thế nào
$nSO_3 + H_2SO_4 \to H_2SO_4.nSO_3$
Theo PTHH : $n_{H_2SO_4} = n_{SO_3} = 1(mol)$
$\Rightarrow n = 1$
Vậy công thức của oleum là $H_2SO_3.SO_3$
Đúng 2
Bình luận (0)