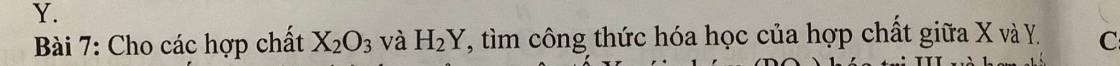Hóa học
P → H3PO4 → Ca3(PO4)2 → Ca(H2PO4)2 → CaHPO4 → Ca3(PO4)2 → H3PO4
\(4P+5O_2\xrightarrow[]{t^o}2P_2O_5\)
`P_2O_5 + 3H_2O -> 2H_3PO_4`
`2H_3PO_4 + 3CaO -> Ca_3(PO_4)_2 + 3H_2O`
`Ca_3(PO_4)_2 + 4H_3PO_4 -> 3Ca(H_2PO_4)_2`
`Ca(H_2PO_4)_2 + Ca(OH)_2 -> 2CaHPO_4 + 2H_2O`
`2CaHPO_4 + Ca(OH)_2 -> Ca_3(PO_4)_2 + 2H_2O`
`Ca_3(PO_4)_2 + 3H_2SO_4 -> 3CaSO_4 + 2H_3PO_4`
Đúng 2
Bình luận (0)
Cho 15,3 gam BaO vào nước thu được 2 lít dung dịch bazo
a. Viết PTHH xảy ra và tính khối lượng mỗi muốn trong hỗn hợp đầu
b. Tính thành phần % khối lượng mỗi muối trong hỗn hợp đầu
c. Tính \(C_M\) của dung dịch HCl
\(n_{BaO}=\dfrac{15,3}{153}=0,1\left(mol\right)\\ a,BaO+H_2O\rightarrow Ba\left(OH\right)_2\\ n_{Ba\left(OH\right)_2}=n_{BaO}=0,1\left(mol\right)\\ \)
KL mỗi muối là sao em?
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 8,1 gam kim loại Al trong dung dịch HCl 14,6% (vừa đủ)
a. Tính thể tích khí thu được ở đktc
b. Tính khối lượng dung dịch HCl cần dùng
c. Tính nồng độ % của dung dịch muối thu được
\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ n_{H_2}=\dfrac{3}{2}.0,3=0,45\left(mol\right)\\ n_{HCl}=\dfrac{6}{2}.0,3=0,9\left(mol\right)\\ n_{AlCl_3}=n_{Al}=0,3\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,45.22,4=10,08\left(l\right)\\ b,m_{ddHCl}=\dfrac{0,9.36,5.100}{14,6}=225\left(g\right)\\ c,C\%_{ddAlCl_3}=\dfrac{0,3.133,5}{8,1+225-0,45.2}.100\%\approx17,248\%\)
Đúng 0
Bình luận (0)
Viết các PTHH theo sơ đồ chuyển hóa sau:
P → P2O5 → H3PO4 → Na3PO4 → Ag3PO4
Ca3(PO4)2 → P → Zn3P2 → PH3
a) \(4P+5O_2\xrightarrow[]{t^o}2P_2O_5\)
`P_2O_5 + 3H_2O -> 2H_3PO_4`
`H_3PO_4 + 3NaOH -> Na_3PO_4 + 3H_2O`
\(Na_3PO_4+3AgNO_3\rightarrow Ag_3PO_4\downarrow+3NaNO_3\)
b) \(5C+Ca_3\left(PO_4\right)_2+3SiO_2\xrightarrow[]{1200^oC}5CO+2P+3CaSiO_3\)
\(3Zn+2P\xrightarrow[]{t^o}Zn_3P_2\)
`Zn_3P_2 + 6HCl -> 3ZnCl_2 + 2PH_3`
Đúng 3
Bình luận (0)
4P+5O2-to>2P2O5
P2O5+3H2O->2H3PO4
H3PO4+3NaOH->Na3PO4+H2O
Na3PO4+3AgNO3->Ag3PO4+3NaNO3
Đúng 2
Bình luận (0)
X2O3 =>O hóa trị 2 ->X hóa trị 3
H2Y =>H hóa trị 1 =>Y hóa trị 2
=>CTTQ : X2Y3
Đúng 2
Bình luận (0)
X2O3 => X(III)
H2Y => Y(II)
=> CTHH X và Y: X2Y3
Đúng 0
Bình luận (0)
Gọi hoá trị của X là x, theo quy tắc hoá trị, ta có:
\(2.x=3.II\Rightarrow y=\dfrac{3.2}{2}=3=III\)
Gọi hoá trị của Y là y, theo quy tắc hoá trị, ta có:
\(2.I=1.y\Rightarrow y=\dfrac{2.1}{1}=2=II\)
Gọi CTTQ của hợp chất giữa X và Y là \(X_aO_b\) (a, b nguyên dương)
Theo quy tắc hoá trị, ta có: \(a.III=b.II\)
\(\Rightarrow\dfrac{a}{b}=\dfrac{2}{3}\)
CTHH của hợp chất là `X_2Y_3`
Đúng 0
Bình luận (0)
Câu 6. Kim loại X tác dụng với H2SO4 loãng giải phóng khí Hidro. Dẫn toàn bộ lượng hidro trên qua ống nghiệm chứa oxit, nung nóng thu được kim loại Y. Hai chất X, Y lần lượt là: A. Ca và Zn B. Mg và Ag C. Na và Mg D. Zn và Cu
Đọc tiếp
Câu 6. Kim loại X tác dụng với H2SO4 loãng giải phóng khí Hidro. Dẫn toàn bộ lượng hidro trên qua ống nghiệm chứa oxit, nung nóng thu được kim loại Y. Hai chất X, Y lần lượt là: A. Ca và Zn B. Mg và Ag C. Na và Mg D. Zn và Cu
Câu 6. Kim loại X tác dụng với H2SO4 loãng giải phóng khí Hidro. Dẫn toàn bộ lượng hidro trên qua ống nghiệm chứa oxit, nung nóng thu được kim loại Y. Hai chất X, Y lần lượt là:
A. Ca và Zn B. Mg và Ag C. Na và Mg D. Zn và Cu
Đúng 1
Bình luận (0)
Cho hỗn hợp X gồm NaHSO4, NaOH , Na2SO4 ( tỷ lệ mol là 1:1:1) vào nước, người ta thu được
dung dịch Y chỉ chứa 28,4 gam Na2SO4. Khối lượng NaOH trong hỗn hợp X là
A. 12 gam.
B. 8 gam.
C. 6 gam.
D. 4 gam.
\(Đặt:n_{NaOH}=n_{NaHSO_4}=n_{Na_2SO_4}=a\left(mol\right)\left(a>0\right)\\ n_{Na_2SO_4\left(cuối\right)}=\dfrac{28,4}{142}=0,2\left(mol\right)\\ NaOH+NaHSO_4\rightarrow Na_2SO_4+H_2O\\ n_{Na_2SO_4\left(cuối\right)}=a+a=2a\left(mol\right)=0,2\left(mol\right)\\ \Leftrightarrow a=0,1\left(mol\right)\\ \Rightarrow m_{NaOH}=40a=4\left(g\right)\\ \Rightarrow Chọn.D\)
Đúng 2
Bình luận (0)
Mn giúp mình câu 12,14,15 với ( gấp lắm ạ)
Câu 4. Cặp chất nào sau đây cùng tồn tại trong dung dịch?A. HCl, KClB. HCl và Ca(OH)2C. H2SO4 và BaOD. NaOH và H2SO4
Đọc tiếp
Câu 4. Cặp chất nào sau đây cùng tồn tại trong dung dịch?
A. HCl, KCl
B. HCl và Ca(OH)2
C. H2SO4 và BaO
D. NaOH và H2SO4
Câu 4. Cặp chất nào sau đây cùng tồn tại trong dung dịch?
A. HCl, KCl
B. HCl và Ca(OH)2
C. H2SO4 và BaO
D. NaOH và H2SO4
Đúng 0
Bình luận (0)