(H+) = 10-2 (M)
⇒ pH = -lg(10-2) = 2
(H+) = 10-2 (M)
⇒ pH = -lg(10-2) = 2
Tính pH của dung dịch có nồng độ OH- là 10-4 M.
Một dung dịch có\({\rm{(O}}{{\rm{H}}^{\rm{ - }}}{\rm{) = 2}}{\rm{,5 x 1}}{{\rm{0}}^{{\rm{ - 10}}}}{\rm{ M}}\). Tính pH và xác định môi trường của dung dịch này.
Một mẫu dịch vị có pH = 2,5. Xác định nồng độ mol của ion H+ trong mẫu dịch vị đó.
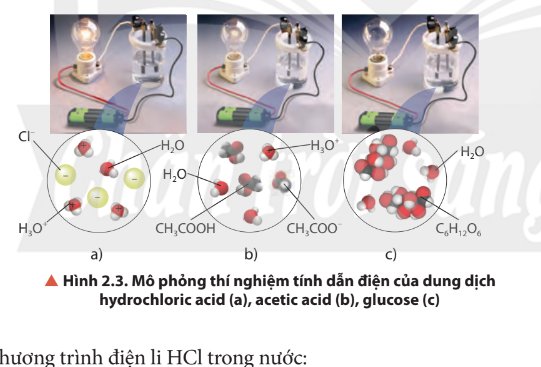
Quan sát Hình 2.3, nhận xét về độ sáng của bóng đèn ở các thí nghiệm. Biết rằng nồng độ mol của các dung dịch là bằng nhau, cho biết dung dịch nào dẫn điện mạnh, dẫn điện yếu và không dẫn điện.
Giả sử khi kết thúc chuẩn độ, thể tích dung dịch NaOH đã sử dụng là 12,5 mL. Tính nồng độ dung dịch NaOH ban đầu.
Tính pH của dung dịch thu được sau khi trộn 40 mL dung dịch HCl 0,5 M với 60 mL dung dịch NaOH 0,5 M.
Các hợp chất acid và base có vai trò rất quan trọng trong đời sống của con người. Acid, base là gì? Làm cách nào có thể xác định nồng độ của dung dịch acid, base?
Quan sát Hình 2.8, trình bày sự chuyển đổi màu sắc của các chất chỉ thị acid – base trong các dung dịch có độ pH khác nhau.

a) Pha 500 mL dung dịch HCl 0,2 M vào 500 mL nước. Tính pH của dung dịch thu được.
b) Tính khối lượng NaOH cần để pha 100 mL dung dịch NaOH có pH = 12.