Bài 32: Phản ứng Oxi hóa - khử
Nội dung lý thuyết
Các phiên bản khácI. SỰ KHỬ, SỰ OXI HÓA
1. Sự khử
Xét phản ứng của hidro với đồng (II) oxit ở nhiệt độ cao
H2 + CuO Cu + H2O (1)
.gif)
Trong phản ứng trên ta thấy nguyên tử oxi đã bị tách ra khỏi phân tử CuO bởi hidro. Ta nói đã xảy ra sự khử CuO thành Cu.
Ở các điều kiện thích hợp khác, khí H2 hay khí CO, C có thể chiếm được nguyên tố oxi của một oxit kim loại khác như kẽm (II) oxit ZnO, chì (II) oxit PbO.... Người ta nói trong các phản ứng này đã xảy ra sự khử (hoặc sự khử oxi) oxit kim loại.
Vậy sự tách oxi ra khỏi hợp chất gọi là sự khử.
2. Sự oxi hóa
Theo định nghĩa sự oxi hóa (bài 25) ta có: Sự oxi hóa là sự tác dụng của oxi với một chất khác.
Trong phản ứng (1) đã xảy ra quá trình kết hợp của nguyên tử oxi trong CuO với phân tử H2, ta nói đã xảy ra sự oxi hóa H2 thành H2O.
@91267@@91266@
II. CHẤT KHỬ VÀ CHẤT OXI HÓA
Trong phản ứng của hidro và đồng (II) oxit CuO ta thấy đã xảy ra sự khử CuO thành Cu, vậy chất khử và chiếm nguyên tử oxi của CuO là hidro. Và ngược lại hidro cũng bị oxi hóa bởi nguyên tử oxi trong phân tử CuO tạo thành H2O nên do đó CuO là chất oxi hóa và nhường oxi cho chất khử là hidro.
Kết luận
- Chất chiếm oxi của chất khác là chất khử.
- Chất nhường oxi cho chất khác là chất oxi hóa.
- Bản thân phân tử oxi cũng là chất oxi hóa.
.png)
@91268@
III. PHẢN ỨNG OXI HÓA - KHỬ
Có thể biểu diễn quá trình oxi hóa và khử trong phản ứng (1) bằng sơ đồ sau:
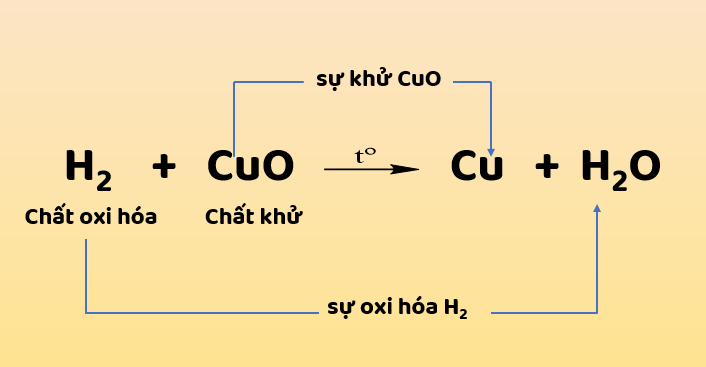
Sự khử và sự oxi hóa là hai quá trình ngược nhau nhưng xảy ra đồng thời trong cùng một phản ứng hóa học. Phản ứng đó gọi là phản ứng oxi hóa - khử.
Định nghĩa: Phản ứng oxi hóa - khử là phản ứng trong đó xảy ra đồng thời sự oxi hóa và sự khử.
@91270@
IV. TỔNG KẾT
1. Chất chiếm oxi của chất khác là chất khử. Chất nhường oxi cho chất khác là chất oxi hóa.
2. Sự tách oxi ra khỏi hợp chất là sự khử. Sự tác dụng của oxi với một chất là sự oxi hóa.
3. Phản ứng oxi hóa - khử là phản ứng hóa học trong đó xảy ra đồng thời sự oxi hóa và sự khử.
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!