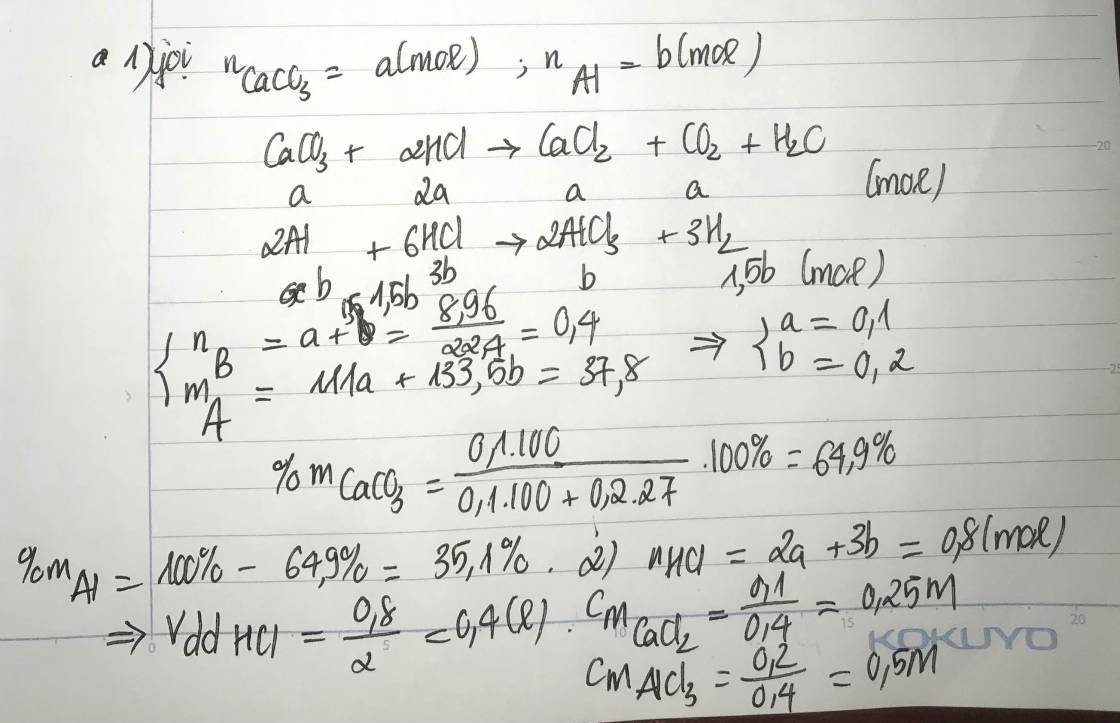Cho m gam hỗn hợp G gồm: CaCO3 và Al vào một lượng vừa đủ V lít ddHCl 2M. Sau phản ứng thu được dung dịch A và 8,96 lít khí B ở đktc. Cô cạn A thu được 37,8 gam muối khan.
1/ Xác định % khối lượng của các chất trong G.
2/ Tính CM của các chất trong A.