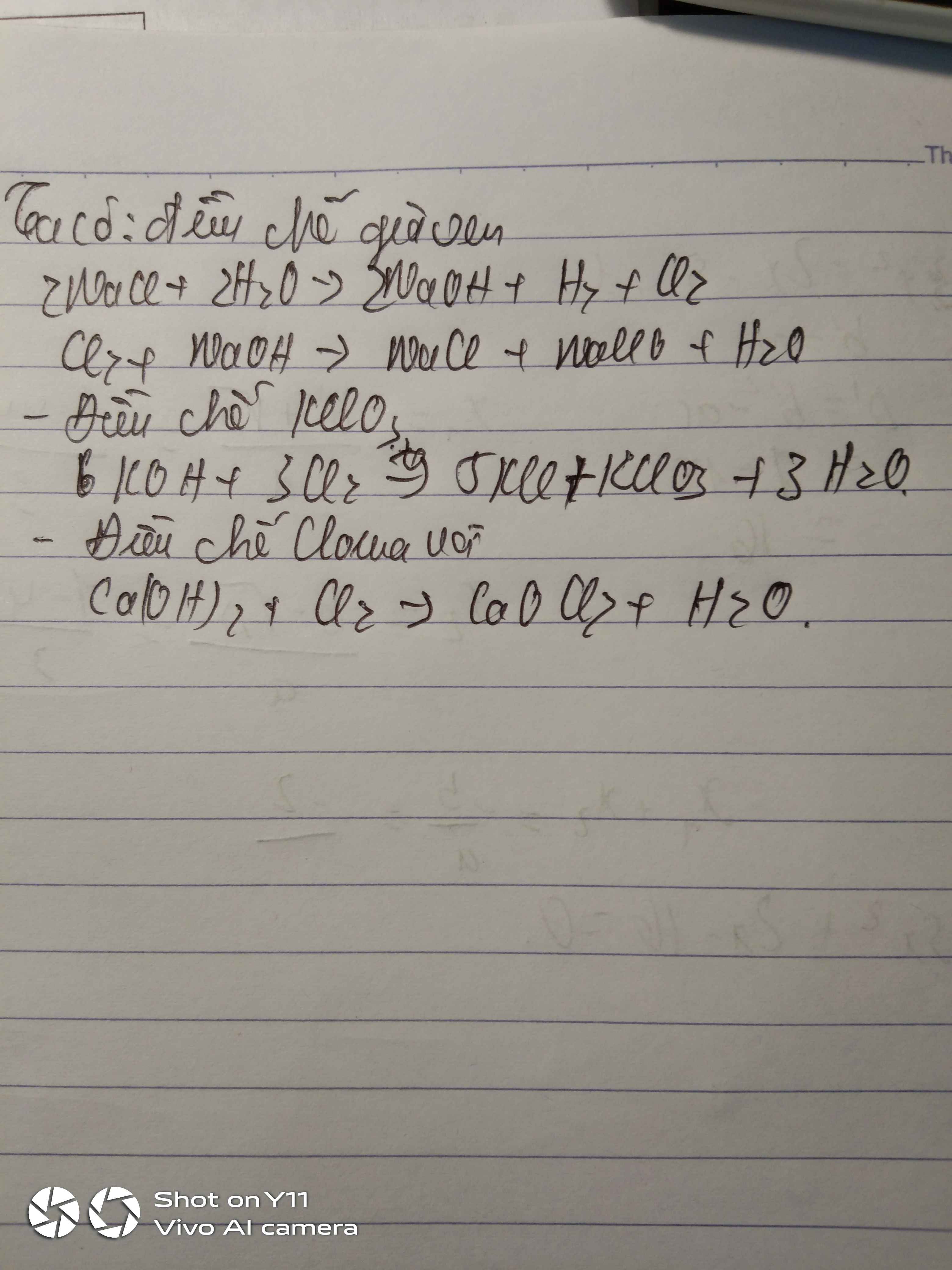Chương 5. Nhóm Halogen
Câu 31:
a, Cl2 + 2Na -> (t°) 2NaCl
2NaCl + H2SO4 -> 2HCl + Na2SO4
MnO2 + 4HCl -> MnCl2 + 2H2O + Cl2
Ca(OH)2 + Cl2 -> CaOCl2 + H2O
b, Cl2 + H2 -> (as) 2HCl
2HCl + NaOH -> NaCl2 + H2O
2NaCl -> (đpnc) 2Na + Cl2
Cl2 + 2NaOH -> NaCl + NaClO + H2O
Đúng 2
Bình luận (0)
Câu 1: viết các phương trình phản ứng xảy ra cho các sơ đồ saua,HCl→Cl2→FeCl3→NaCl→HCl→CuCl2→AgClb,KMnO4→Cl2→HCl→FeCl3→AgCl→Cl2→Br2→I2→ZnI2→Zn(OH)2c,MnO2→Cl2→KClO3→KCl→HCl→Cl2→Clorua vôiCâu 2: Nhận biết các dạng dung dịch mất nhãn sau bằng phương pháp hóa học :NaCl,NaBr,NaI,HCl,H2SO4,NaOH.Câu 3: Cho 31,6 g KMnO4 tác dụng với dung dịch HCl dư sẽ thu được bao nhiêu lít Cl2(ở đktc) nếu H của phản ứng là 75 %Câu 4: Cho 8,3 gam hỗn hợp Al,Fe,Mg tác dụng hết với dung dịch HCl vừa đủ .Sau phản ứng khối...
Đọc tiếp
Câu 1: viết các phương trình phản ứng xảy ra cho các sơ đồ sau
a,HCl→Cl2→FeCl3→NaCl→HCl→CuCl2→AgCl
b,KMnO4→Cl2→HCl→FeCl3→AgCl→Cl2→Br2→I2→ZnI2→Zn(OH)2
c,MnO2→Cl2→KClO3→KCl→HCl→Cl2→Clorua vôi
Câu 2: Nhận biết các dạng dung dịch mất nhãn sau bằng phương pháp hóa học :NaCl,NaBr,NaI,HCl,H2SO4,NaOH.
Câu 3: Cho 31,6 g KMnO4 tác dụng với dung dịch HCl dư sẽ thu được bao nhiêu lít Cl2(ở đktc) nếu H của phản ứng là 75 %
Câu 4: Cho 8,3 gam hỗn hợp Al,Fe,Mg tác dụng hết với dung dịch HCl vừa đủ .Sau phản ứng khối lượng dung dịch HCl tăng thêm 7,8 gam . Tính khối lượng muối thu được.
Câu 5: Hỗn hợp khí X gồm o6zon và oxi có tỉ khối đối với hidro bằng 17,2. Tính phần trăm theo thể tích mỗi khí trong hỗn hợp X.
Câu 6:Cho 9 gam hỗn hợp gồm Al và Cu tác dụng với lượng dư dung dịch HCl nồng độ 20% . Sau phản ứng thu được 1,344 lít khí (ở đktc).
a, Tính % về khối lượng các kim loại trong hỗn hợp ban đầu
b,Tính khối lượng dung dịch HCl đã dùng . Biết rằng lượng dung dịch HCl đã dùng được lấy dư 10% so với lượng cần thiết cho phản ứng.
tách nhỏ ra bạn nhé, 1 lần bạn đăng 1 câu thôi nhé!
Đúng 0
Bình luận (2)
Mình làm câu 2 nhé:
Cho thử quỳ tím:
- Quỳ tím chuyển đỏ -> H2SO4, HCl (1)
- Quỳ tím chuyển xanh -> NaOH
- Quỳ tím không đổi màu -> NaCl, NaI, NaBr (2)
Cho lần lượt các chất (1) tác dụng với BaCl2:
- Xuất hiện kết tủa trắng -> H2SO4
BaCl2 + H2SO4 -> BaSO4 + 2HCl
- Không hiện tượng -> HCl
Cho lần lượt các chất (2) tác dụng với AgNO3:
- Kết tủa màu trắng -> AgCl
NaCl + AgNO3 -> AgCl + NaNO3
- Kết tủa màu vàng nhạt -> NaBr
NaBr + AgNO3 -> NaNO3 + AgBr
Kết tủa màu vàng đậm -> NaI
NaI + AgNO3 -> AgI + NaNO3
Đúng 2
Bình luận (2)
Cho 20.0 gam oxit kim loại tác dụng vừa đủ với 500ml dd HCl 2M phần trăm khối lượng kim loại trong oxit là
\(n_{HCl}=2.0,5=1\left(mol\right)\)
=> nH2O = 0,5 (mol)
=> nO = 0,5 (mol)
=> mKL = 20 - 0,5.16 = 12 (g)
=> \(\%m_{KL}=\dfrac{12}{20}.100\%=60\%\)
Đúng 2
Bình luận (0)
Hỗn hợp A gồm 3 muối NaCl, NaBr, NaI. Cho 5,76 gam A tác dụng với lượng dư dung dịch Br2 cô cạn thu được 5,29g muối khan. Hòa tan 5,76 gam A vào nước rồi cho một lượng khí Clo sục qua dung dịch. Sau một thời gian cô cạn thì thu được 3,955 gam muối khan. a. Viết các PTHH b. Tính thành phần % mỗi muối trong A.
\(\left\{{}\begin{matrix}nNaCl=x\\nNaBr=y\\nNaI=z\end{matrix}\right.\)
ta có : \(58,5x+103y+150z=5,76\left(1\right)\)
TN1:
\(Br_2+2NaI\rightarrow2NaBr+I_2\)
z ----> z
\(\Rightarrow m_{muối}=mNaBr+mNaCl=103\left(y+z\right)+58,5x=5,29\left(2\right)\)
Từ (1) và (2) => z =0,01
TN2:
\(Cl_2+2NaI\rightarrow2NaCl+I_2\)
0,01 0,01
\(Cl_2+2NaBr\rightarrow2NaCl+I_2\)
\(nNaCl=nCl^-=0,05\rightarrow mNaCl=2,925\left(g\right)\)muối khan ngoài NaCl còn muối khác.Do \(I^-\) có tính khử mạnh hơn \(Br^-\) nên NaI sẽ hết trước và sau hai phản ứng NaBr còn dư.
\(nNaBr\left(dư\right)=t\)
\(\Rightarrow nNaCl=0,05=0,01+y-t+x\)
\(m_{muối}=mNacl+mNaBr\Rightarrow mNaBr_{\left(dư\right)}=3,955-0,05.58,5=1,03\)
\(\Rightarrow t=0,01\)
\(\Rightarrow x+y=0,05\left(3\right)\)
(1) ; (3) ; => \(x=0,02;y=0,03\)
\(\Rightarrow mNaCl=1,17\left(g\right)\)
Đúng 1
Bình luận (0)
nêu hiện tượng và viết phương trình xảy ra trong các trường hợp sau:
a) thêm từ từ nước clo vào dung dịch kali iotua có chứa sẵn một ít hồ tinh bột.
b) nhỏ dung dịch axit flohiđric vào bình thủy tinh và để một thời gian.
a) dd chuyển màu xanh tím
\(2KI+Cl_2\rightarrow2KCl+I_2\) (I2 làm xanh hồ tinh bột)
b) Bình thủy tinh dần bị ăn mòn:
\(SiO_2+4HF\rightarrow SiF_4+2H_2O\)
Đúng 5
Bình luận (0)
Hòa tan 104,25g hỗn hợp các muối NaCl và NaI vào nước. Cho đủ khí clo đi qua rồi đun cạn. Nung chất rắn thu được cho hết hơi màu tím bay ra, bã rắn còn lại sau khi nung nặng 58,5g. Tính % khối lượng NaCl trong hỗn hợp đầu?
Gọi x, y là số mol NaCl và NaI trong hh X
m(X) = m(NaCl) + m(NaI) = 58,5x + 150y = 104,25g (1)
Sục khí Cl2 dư vào dd A:
NaI + 1/2Cl2 → 1/2I2 + NaCl
y → y
mmuối = m(NaCl) = 58,5.(x+y) = 58,5g
→ x + y = 1mol (2)
Giải hệ PT (1), (2) ta được: x = 0,5mol và y = 0,5mol
mNaCl = 0.5.58,5 = 29,25 (g)
=>%m NaCl=\(\dfrac{29,25}{102,25}\).100=28,05%
Đúng 2
Bình luận (0)
NaCl + Cl2 → không phản ứng
a
2NaI + Cl2 → 2NaCl + I2 (1)
b b
mNaCl + mNaI = 104,25 = 58,5a + 150b
Chất rắn còn lại sau nung gồm NaCl không phản ứng và NaCl là sản phẩm của phản ứng (1)
nNaCl = a + b = 1
→ a = 0,5, b = 0,5 → mNaCl ban đầu = 0,5.58,5 = 29,25 gam
→ %mNaCl = 28,06%
Đúng 1
Bình luận (0)
Cho các chất: NaCl, KMnO4, KOH, NaOH, Ca(OH)2, H2SO4, H2O. Từ các hóa chất đã cho, viết các phương trình hóa họcxảy ra khi điều chế các chất sau trong phòng thí nghiệm: a. nước giaven. b. clorua vôi.c. kaliclorat.
Đọc tiếp
Cho các chất: NaCl, KMnO4, KOH, NaOH, Ca(OH)2, H2SO4, H2O. Từ các hóa chất đã cho, viết các phương trình hóa họcxảy ra khi điều chế các chất sau trong phòng thí nghiệm:
a. nước giaven. b. clorua vôi.c. kaliclorat.
a) Nước Gia-ven:
\(2NaCl+H_2O\underrightarrow{đpkmn}NaCl+NaClO+H_2\)
b) Clorua vôi
\(2NaCl+2H_2O\underrightarrow{đpcmn}2NaOH+H_2+Cl_2\)
\(Cl_2+Ca\left(OH\right)_2\rightarrow CaOCl_2+H_2O\)
c)
\(6KOH+3Cl_2\underrightarrow{t^o}5KCl+KClO_3+3H_2O\)
Đúng 3
Bình luận (0)
Nhận biết các dd sau HCL HNO3
Cho AgNO3 tác dụng với từng chất:
- Tạo kết tủa trắng bạc -> HCl
- Không hiện tượng -> HNO3
Đúng 2
Bình luận (0)
Ta nhỏ AgNO3
Có kết tủa trắng là HCl
Còn lại ko hiện tượng là HNO3
HCl+AgNO3->AgCl+HNO3
Đúng 2
Bình luận (0)
Chất nào đây được dùng để diệt trùng nước sinh hoạt?
A,Clo.
B,Brom.
C,Oxi.
D,Nitơ.
Xem thêm câu trả lời
Ở nhiệt độ thường, chất nào sau đây là chất lỏng màu đỏ nâu?
A,F2
VMBr2
C,I2
D,Cl2
Xem thêm câu trả lời