Câu 29. Xác định pH của dung dịch sau khi trộn 100 ml KOH 0,01 M, 100 ml CH3COOH 0,02 M và 10 ml NaOH 0,015 M, biết pKaCH3COOH = 4,75 GIÚP EM CÂU NÀY VỚI Ạ
Chương 1. Sự điện li
Trộn 200 ml dung dịch HCl 1M với 300 ml dung dịch HCl 2M thì thu được dung dịch X. Trộn 400 ml dung dịch X trên với 600 ml dung dịch Y gồm NaOH 0,5M và Ba(OH)2 nồng độ 0,5M. Phản ứng kết thúc thu được dung dịch Z. Cô cạn dung dịch Z thu được m gam chất rắn. Tính m và nồng độ mol các ion có trong Z
Thổi CO2 vào dung dịch Ca(OH)2 dư, khi kết thúc phản ứng A. thu được kết tủa màu trắng. B. thu được dung dịch trong suốt C. được kết tủa và có khí thoát ra. D. thấy dung dịch bị đổi màu.
cho các dd NaCL, NaOH, HNO3, Ba(OH)2 có cùng nồng độ mol, dd có pH lớn nhất là
Tính pH của dung dịch thu được sau khi trộn 100 ml dd KOH 0,02M với 100ml dd HCl 0,01M
\(n_{OH-}=0.1\cdot0.02=0.002\left(mol\right)\)
\(n_{H+}=0.01\cdot0.1=0.001\left(mol\right)\)
=>OH- dư 0,001mol
\(\left[OH^-\right]=\dfrac{0.001}{0.2}=5\cdot10^{-3}\left(M\right)\)
=>POH=2,3
=>PH=14-2,3=11,7
Đúng 2
Bình luận (0)
Viết pt dạng phân tử và ion rút gọn của các phản ứng sau
Ba(OH)2 + H2SO4
(NH4)2So4+Bacl2
NaF+HCL
Na2Co3+Ca(NO3)
CuSo4+Na2S
NaHCO3+HCL
NaHCo3 + NaOH
HCLO+Na2S
FeS +HCL
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_{4\downarrow}+H_2O\)
→ \(Ba^{2+}+2OH^-+2H^++SO_4^{2-}\rightarrow BaSO_{4\downarrow}+H_2O\)
\(\left(NH_4\right)_2SO_4+BaCl_2\rightarrow2NH_4Cl+BaSO_{4\downarrow}\)
→ \(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_{4\downarrow}\)
\(NaF+HCl\rightarrow NaCl+HF\)
→ \(F^-+H^+\rightarrow HF\)
\(Na_2CO_3+Ca\left(NO_3\right)_2\rightarrow2NaNO_3+CaCO_{3\downarrow}\)
→ \(CO_3^{2-}+Ca^{2+}\rightarrow CaCO_{3\downarrow}\)
\(CuSO_4+Na_2S\rightarrow Na_2SO_4+CuS_{\downarrow}\)
→ \(Cu^{2+}+S^{2-}\rightarrow CuS_{\downarrow}\)
\(NaHCO_3+HCl\rightarrow NaCl+CO_2+H_2O\)
→ \(HCO_3^-+H^+\rightarrow CO_2+H_2O\)
\(NaHCO_3+NaOH\rightarrow Na_2CO_3+H_2O\)
→ \(HCO_3^-+OH^-\rightarrow CO_3^{2-}+H_2O\)
\(2HClO+Na_2S\rightarrow2NaClO+H_2S\)
→ \(2H^++S^{2-}\rightarrow H_2S\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
→ \(FeS+2H^+\rightarrow Fe^{2+}+H_2S\)
Đúng 1
Bình luận (0)
Cho 50ml dung dịch A gồm Na+, SO42-, CO32-, NH4+ . Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch A và đun nóng thu được 0,34 (g) khí có thể làm xanh giấy quỳ tím ẩm và có 4,3 (g) kết tủa. Còn khi cho A tác dụng với dung dịch H2SO4 loãng dư thì thu được 0,224(l) khí ở đktc. a. Tính nồng độ mol của mỗi ion trong A b. Tính khối lượng muối khan thu được khi cô cạn dung dịch A
Đọc tiếp
Cho 50ml dung dịch A gồm Na+, SO42-, CO32-, NH4+ . Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch A và đun nóng thu được 0,34 (g) khí có thể làm xanh giấy quỳ tím ẩm và có 4,3 (g) kết tủa. Còn khi cho A tác dụng với dung dịch H2SO4 loãng dư thì thu được 0,224(l) khí ở đktc.
a. Tính nồng độ mol của mỗi ion trong A
b. Tính khối lượng muối khan thu được khi cô cạn dung dịch A
Cho dung dịch G chứa các ion Mg2+, SO42-, NH4+, Cl-. Chia dung dịch G thành 2 phần bằng nhau. Phần thứ nhất tác dụng với dd NaOH dư, đun nóng, được 0,58g kết tủa và 0,672 lít khí ở đktc. Phần 2 tác dụng với dung dịch BaCl2 dư, được 4,66g kết tủa tổng khối lượng của chất tan trong dd G là:
Đọc tiếp
Cho dung dịch G chứa các ion Mg2+, SO42-, NH4+, Cl-. Chia dung dịch G thành 2 phần bằng nhau. Phần thứ nhất tác dụng với dd NaOH dư, đun nóng, được 0,58g kết tủa và 0,672 lít khí ở đktc. Phần 2 tác dụng với dung dịch BaCl2 dư, được 4,66g kết tủa tổng khối lượng của chất tan trong dd G là:
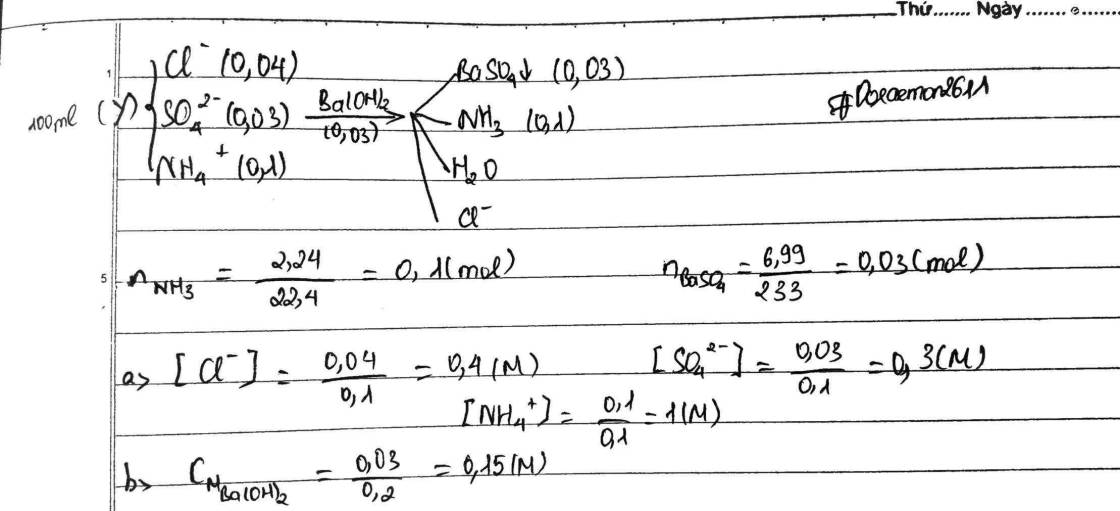
một dd Y chứa các ion Cl-, SO42-, NH4+ Khi cho 100 ml dd Y phản ứng vừa đủ với 200 ml dd Ba(OH)2 thu được 6,99g kết tủa và thoát ra 2,24 lít khí ở đktc.a)Nồng độ mol của các ion trong dd Y lần lượt là:?b)Tính nồng độ mol của dd Ba(OH)2 đã dùng ?
Đọc tiếp
một dd Y chứa các ion Cl-, SO42-, NH4+ Khi cho 100 ml dd Y phản ứng vừa đủ với 200 ml dd Ba(OH)2 thu được 6,99g kết tủa và thoát ra 2,24 lít khí ở đktc.
a)Nồng độ mol của các ion trong dd Y lần lượt là:?
b)Tính nồng độ mol của dd Ba(OH)2 đã dùng ?
dd A chứa các ion NH4+ , Fe3+, SO2-. Cho KOH dư vào 200 ml dd A thu được 1,12 lít khí ở đktc và 10,7g kết tủa nâu đỏ. Khối lượng kết tủa tạo thành khi cho BaCl2 dư vào 400 ml dd A là?