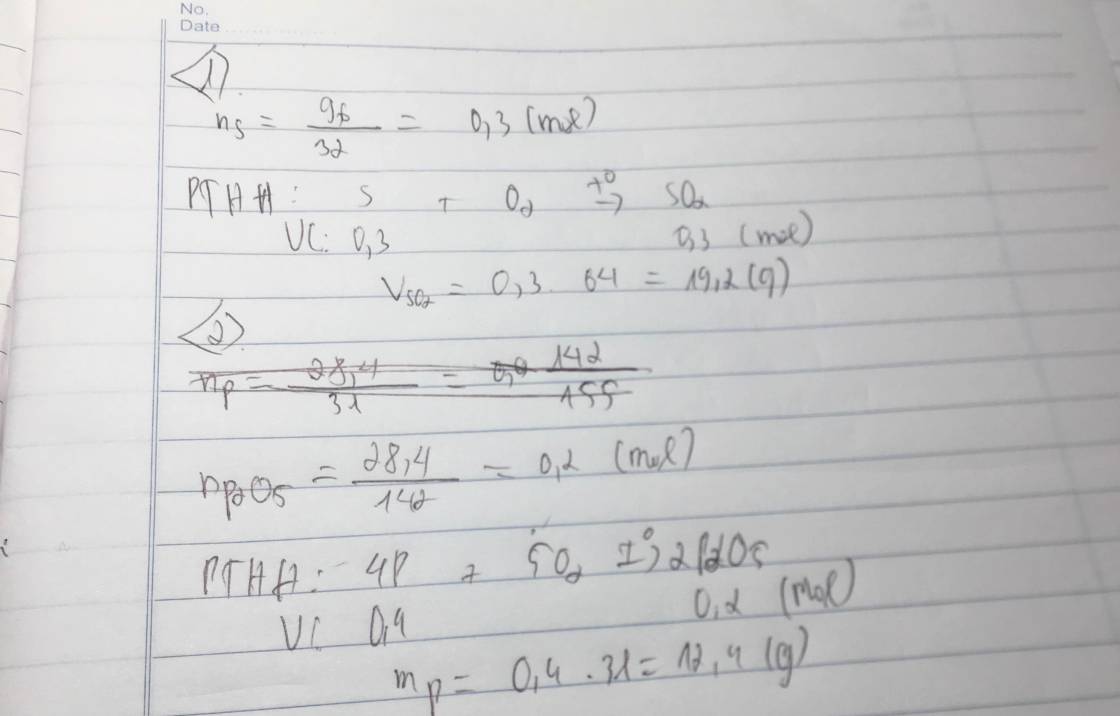Ở nhiệt độ cao, P phản ứng với O2 tạo thành PO2O5. Tính khối lượng P cần dùng để sản xuất được 28,4 gam P2O5
Cho P=31; O=16
Bài 22: Tính theo phương trình hóa học
\(PTPU:4P+5O_2\rightarrow2P_2O_5\)(đk:\(t^o\))
4 : 5 : 2 (tỉ lệ mol)
0,4 0,2 (mol)
\(n_{P_2O_5}=\dfrac{m}{M}=\dfrac{28,4}{\left(2.31+16.5\right)}=0,2\left(mol\right)\)
\(m_P=n.M=0,4.3112,4\left(g\right)\)
Đúng 0
Bình luận (1)
Ở nhiệt độ cao, S phản ứng với O2 tạo thành SO2. Tính thể tích khí SO2 khi dùng 9,6 gam S
Cho S=32; O=16
Ta có: \(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
PT: \(S+O_2\underrightarrow{t^o}SO_2\)
Theo PT: \(n_{SO_2}=n_S=0,3\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,3.24,79=7,437\left(l\right)\)
Đúng 2
Bình luận (0)
\(PTPỨ:S+O_2\rightarrow SO_2\)(đk:\(t^o\))
\(1\) : \(1\) : \(1\) (tỉ lệ mol)
\(0,3\) \(0,3\) (mol)
\(n_S=\dfrac{m}{M}=\dfrac{9,6}{32}0,3\left(mol\right)\)
\(V_{SO_2}=n.22,4=0,3.22,46,72\left(l\right)\)
Đúng 1
Bình luận (0)
Bài 9:
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{O_2}=\dfrac{9,916}{24,79}=0,4\left(mol\right)\)
Theo PT: \(n_{KMnO_4}=2n_{O_2}=0,8\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,8.158=126,4\left(g\right)\)
Bài 10:
PT: \(2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\)
Ta có: \(n_{KClO_3}=\dfrac{1045,8}{122,5}=\dfrac{1494}{175}\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{KClO_3}=\dfrac{2241}{175}\left(mol\right)\)
\(\Rightarrow V_{O_2}=\dfrac{2241}{175}.24,79\approx317,45\left(l\right)\)
Đúng 2
Bình luận (1)
Bài 6:
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Ta có: \(n_{Fe_3O_4}=\dfrac{56}{232}=\dfrac{7}{29}\left(mol\right)\)
Theo PT: \(n_{O_2}=2n_{Fe_3O_4}=\dfrac{14}{29}\left(mol\right)\)
\(\Rightarrow V_{O_2}=\dfrac{14}{29}.24,79\approx11,97\left(l\right)\)
Bài 7:
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Ta có: \(n_{CH_4}=\dfrac{14,874}{24,79}=0,6\left(mol\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}=1,2\left(mol\right)\)
\(\Rightarrow V_{O_2}=1,2.24,79=29,748\left(l\right)\)
Bài 8:
PT: \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
Ta có: \(n_{CaO}=\dfrac{39,2}{56}=0,7\left(mol\right)\)
Theo PT: \(n_{H_2O}=n_{CaO}=0,7\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,7.18=12,6\left(g\right)\)
Đúng 1
Bình luận (0)
Ở nhiệt độ cao, CuO phản ứng với H2 tạo thành Cu và H2O. Tính khối lượng Cu thu được khi sử dụng 16 gam CuO.
Cho Cu=64; O=16; H=1
\(n_{CuO}=0,2\left(mol\right)\)
\(CuO+H_2\xrightarrow[]{t^\circ}Cu+H_2O \)
0,2 → 0,2
\(\Rightarrow m_{Cu}=0,2\cdot64=12,8\left(g\right)\)
Đúng 4
Bình luận (0)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,1 0,1
\(n_{CuO}=\dfrac{16}{160}=0,1\left(mol\right)\)
\(m_{Cu}=0,1.64=6,4\left(g\right)\)
Đúng 0
Bình luận (1)
Tính khối lượng của 7,437 lít khí SO3
\(n_{SO_3\left(dkc\right)}=\dfrac{V}{24,79}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\\ m_{SO_3}=n\cdot M=0,3\cdot\left(32+16\cdot3\right)=24\left(g\right)\)
Đúng 1
Bình luận (0)
\(n_{SO_3}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\\ m_{SO_3}=80.0,3=24\left(g\right)\)
Đúng 0
Bình luận (0)
Tính khối lượng của 0,2479 lít khí N2O
\(n_{N_2O}=\dfrac{V_{N_2O}}{24,79}=\dfrac{0,2479}{24,79}=0,01\left(mol\right)\)
\(m_{N_2O}=n_{N_2O}
.
M_{N_2O}=0,01
.
\left(14
.
2+16\right)=0,01
.
44=0,44\left(g\right)\)
Đúng 2
Bình luận (0)
\(n_{N_2O\left(dkc\right)}=\dfrac{V}{24,79}=\dfrac{0,2479}{24,79}=0,01\left(mol\right)\\ m_{N_2O}=n\cdot M=0,01\cdot\left(14\cdot2+16\right)=0,44\left(g\right)\)
Đúng 2
Bình luận (2)
nN2O = \(\dfrac{0,2479}{22,4}\)
nN2O = 0,01 ( mol )
mN2O= MN2O.nN2O
mN2O = 0,01 . 44 = 0,44 ( g/mol )
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Tính khối lượng của 24,79 lít khí CO
\(n_{CO\left(dkc\right)}=\dfrac{V}{24,79}=\dfrac{24,79}{24,79}=1\left(mol\right)\\ m_{CO}=n\cdot M=1\cdot\left(12+16\right)=28\left(g\right)\)
Đúng 1
Bình luận (0)
nCO= \(\dfrac{24,79}{22,4}\)
nCO=1,11 ( mol )
mCO= 1,11.28
mCO= 31,08 ( mol/g)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời