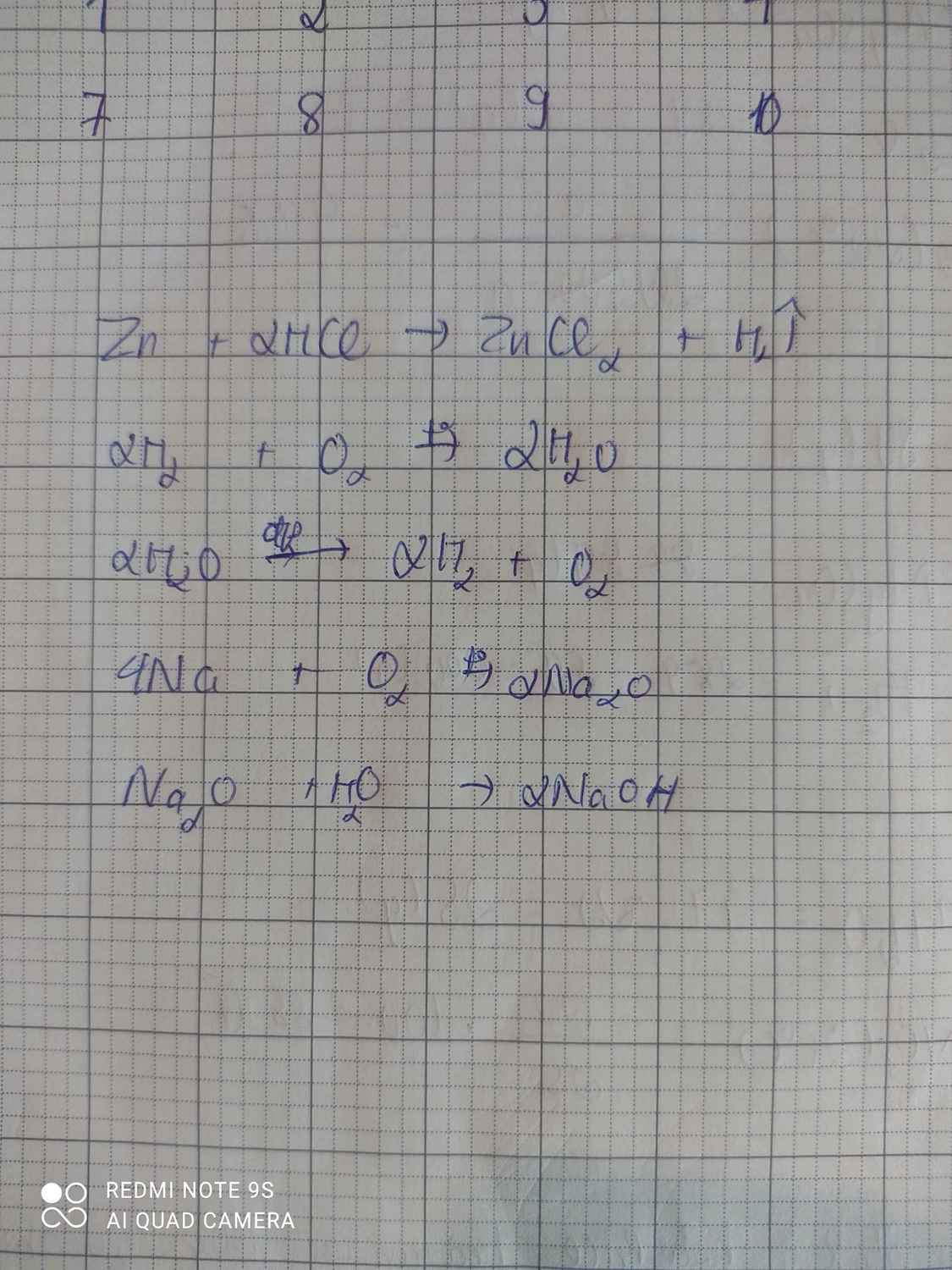Bài 16: Phương trình hóa học
Oxit phi kim nào dưới đây không phải là oxit axit?
A.
SO 2 .
B.
SO 3 .
C.
NO.
D.
N 2 O 5 .
Xem thêm câu trả lời
Phản ứng nào sau đây là phản ứng hóa hợp?A. 2KMnO 4 K 2 MnO 4 + MnO 2 + O 2 .B.CaO + CO 2 → CaCO 3 .C. 2HgO 2Hg + O 2 .D. Cu(OH) 2 CuO + H 2 O
Đọc tiếp
Phản ứng nào sau đây là phản ứng hóa hợp?
A. 2KMnO 4

K 2 MnO 4 + MnO 2 + O 2 .
B.
CaO + CO 2 → CaCO 3 .
C. 2HgO

2Hg + O 2 .
D. Cu(OH) 2

CuO + H 2 O
Cái đề của bạn bị sao rồi bạn ơi!!!!!!!!
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho 13g Zn tác dụng với 0,3 mol HCl sau khi kết thúc phản ứng thu được muối kẽm Clorua và khí H 2. Thể tích khí hidro thu được ở đktc là:
A.
5,6 l.
B.
22,4l.
C.
11,2 l.
D.
3,36 l.
Ta có: nZn = \(\dfrac{13}{65}\) = 0,2 mol
PTHH : Zn + 2HCl → ZnCl2 + H2
ban đầu : 0,2 0,3
phản ứng : 0,15 0,3 0,15
sau phản ứng : 0,05 0 0,15
→ nH2 = 0,15 mol
=> VH2 = 0,15 . 22,4 = 3,36 lít
Đáp án đúng là D bạn nhé
Đúng 4
Bình luận (1)
PTHH:
2Al + 3H2(SO4)3 -> Al2(SO4)3 + 3H2O
Zn + 2HCl -> ZnCl2 + H2
2Al + 3CuCl2 -> 2AlCl3 + 3Cu
H2O + Na2O -> 2NaOH
Phản ứng hóa hợp: d
Phản ứng thế: a, b, c
Đúng 1
Bình luận (0)
bằng phương pháp hóa học em hãy nhận biết các lọ không nhãn đựng các chất khí sau: Oxi, Cacbonđi oxít, Hiđrô
THAM KHẢO CỦA CJ LINH
Trích mẫu thử
Cho que đóm đang cháy vào các mẫu thử
- mẫu thử nào làm que đóm tắt là CO2
- mẫu thử nào làm que đóm tiếp tục cháy là O2
- mẫu thử nào làm que đóm cháy với ngọn lửa màu xanh nhạt là H2
Đúng 3
Bình luận (3)
khử 9,6 gam đồng (ll) oxit bằng khí hiđro. hãy:
a)tính số gam đồng kim loại thu được;
b)tính thể tích khí hiđro (đktc)cần dùng.
\(n_{CuO}=\dfrac{9,6}{80}=0,12mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,12 0,12 0,12
a)\(m_{Cu}=0,12\cdot64=7,68g\)
b)\(V=0,12\cdot22,4=2,688l\)
Đúng 2
Bình luận (0)
\(n_{CuO}=\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{9,6}{80}=0,12mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,12 0,12 0,12 ( mol )
\(m_{Cu}=n_{Cu}.M_{Cu}=0,12.56=6,72g\)
\(V_{H_2}=n_{H_2}.22,4=0,12.22,4=2,688l\)
Đúng 1
Bình luận (0)
Câu 1. Lập phương trình hóa học của các phản ứng sau:a. Al + O2 --to …b. … + O2 --to N2O5c. … + … --to Fe3O4 d. KClO3 -to KCl + …e. KMnO4 -to … + MnO2 + …f. C2H6O + … -to CO2 + H2Og. Al + H2SO4 loãng → … + H2h. Fe + … → FeCl2 + H2i. Fe3O4 + … -to Fe + …k. … + … -to H2OMỗi phản ứng hóa học trên đây thuộc loại phản ứng hóa học nào?...
Đọc tiếp
Câu 1. Lập phương trình hóa học của các phản ứng sau:
a. Al + O2 -->to …
b. … + O2 -->to N2O5
c. … + … -->to Fe3O4
d. KClO3 ->to KCl + …
e. KMnO4 ->to … + MnO2 + …
f. C2H6O + … ->to CO2 + H2O
g. Al + H2SO4 loãng → … + H2
h. Fe + … → FeCl2 + H2
i. Fe3O4 + … ->to Fe + …
k. … + … ->to H2O
Mỗi phản ứng hóa học trên đây thuộc loại phản ứng hóa học nào? (Phản ứng: hóa hợp, phân hủy, phản ứng có xảy ra sự oxi hóa chất, thế)
a) Al + O2 → Al2O3
b) N2 + O2 → N2O5
c) Fe + O2 → Fe3O4
d) KClO3 → KCl + O2
e) KMnO4 → K2MnO4 + MnO2 + O2
f) C2H6O + O2 → CO2 + H2O
g) Al + H2SO4 loãng → Al2(SO4)3 + H2
h) Fe + HCl → FeCl2 + H2
i) Fe3O4 + H2 → Fe + H2O
k) H2 + O2 → H2O
(tất cả các phản ứng trên chưa cân bằng)
Phản ứng hoá hợp: a, b, c, k
Phản ứng phân huỷ: d, e
Phản ứng thế: g, h
Phản ứng có sự oxi hoá chất: a, b, c, f, k
Đúng 3
Bình luận (1)
a) 4Al + 3O2 -> (t°) 2Al2O3
b) 2N2 + 5O2 -> (t°) 2N2O5
c) 3Fe + 2O2 -> (t°) Fe3O4
d) 2KClO3 -> (t°, MnO2) 2KCl + 3O2
e) 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
f) C2H6O + 3O2 -> (t°) 2CO2 + 3H2O
g) 2Al + 3H2SO4 (loãng) -> Al2(SO4)3 + 3H2
h) Fe + HCl -> FeCl2 + H2
i) Fe3O4 + 4H2 -> (t°) 3Fe + 4H2O
k) 2H2 + O2 -> (t°) 2H2O
Phản ứng hoá hợp: a, b, c, k
Phản ứng phân huỷ: d, e
Phản ứng thế: g, h
Phản ứng có sự oxi hoá chất: a, b, c, f, k
Đúng 0
Bình luận (1)
Bài tập này làm kiểu gì
Viết phương trình hoá học thực hiện chuỗi phản ứng sau:
Zn → H2 → H2O → O2 → Na2O → NaOH
Zn+H2SO4->ZnSO4+H2
2H2+O2-to>2H2O
2H2O-đp->H2+O2
O2+4Na-to>2Na2O
Na2O+H2O->2NaOH
Đúng 3
Bình luận (0)
\(Zn+H_2SO_4\rightarrow\left(t^o\right)ZnSO_4+H_2\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
\(2H_2O\underrightarrow{đp}2H_2+O_2\)
\(4Na+O_2\rightarrow\left(t^o\right)2Na_2O\)
\(Na_2O+H_2O\rightarrow2NaOH\)
Đúng 1
Bình luận (4)