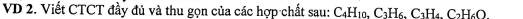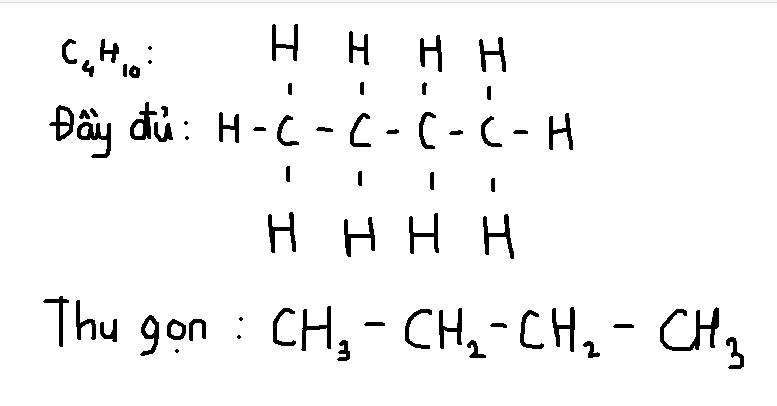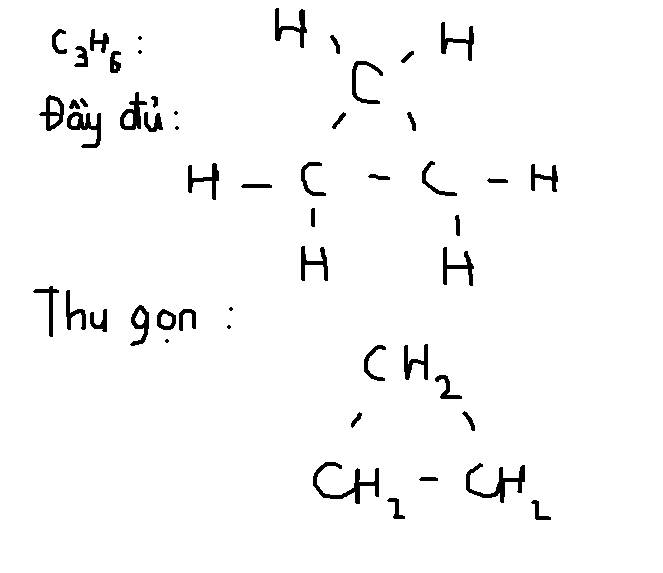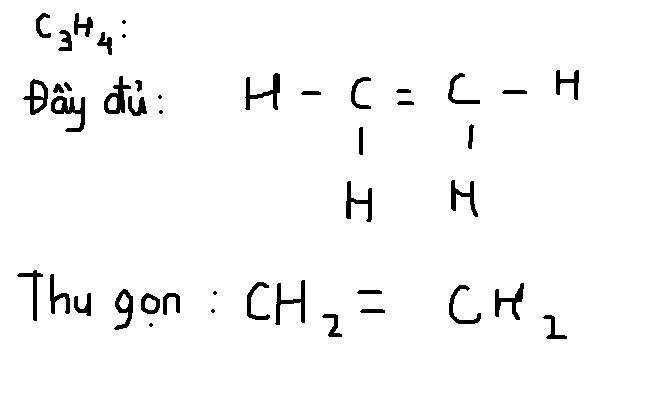Trình bày phương pháp hóa học để : Tách lấy khí metan từ hỗn hợp etilen, axetilen, cacbonic
Hóa học
- Dẫn hỗn hợp khí qua dd Br2 dư, dd thu được gồm CH4 và CO2.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
- Dẫn hỗn hợp khí thu được ở trên qua nước vôi trong dư, thu được CH4 bay ra.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Đúng 1
Bình luận (0)
Cho dòng khí H2 dư đi qua 27,2 gam hỗn hợp bột CuO và một oxide sắt nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được 20 gam chất rắn và m gam nước. Cho lượng chất rắn thu được tác dụng với dung dịch HCl dư, thu được m1 gam chất răn không tan và 7,437 lít khí H2 (đkc). a) Xác định ct của sắt oxide. b) Tính m và m₁.
a, nH2 = 0,3 (mol)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
⇒ nFe = nH2 = 0,3 (mol)
\(\Rightarrow n_{Cu}=\dfrac{20-0,3.56}{64}=0,05\left(mol\right)\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: nCuO = nCu = 0,05 (mol)
⇒ mO (trong oxit sắt) = 27,2 - mCuO - mFe = 6,4 (g)
⇒ nO (trong oxit sắt) = 0,4 (mol)
Gọi CT cần tìm là FexOy
⇒ x:y = 0,3:0,4 = 3:4
Vậy: CT oxit sắt đó là Fe3O4.
b, Gọi: nH2O = x (mol)
Có: H2 + O → H2O
⇒ nH2 = nH2O = x (mol)
BTKL, có: 27,2 + 2x = 20 + 18x
⇒ x = 0,45 (mol)
⇒ m = mH2O = 0,45.18 = 8,1 (g)
m1 = mCu = 0,05.64 = 3,2 (g)
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 2g chất hữu cơ A thu được 3,36 là CO2(đktc)và và 3,6g h2o biết khối lượng của bằng 60g/mlo
a,lập ctpt của A
b, biết rằng A có thể phải có phản ứng vớ
đốt cháy hoàn toàn 72 gam hợp chất hộp athu
a, Ta có: \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
⇒ mC + mH = 0,15.12 + 0,4.1 = 2,2 (g) > mA → vô lý
Bạn xem lại đề nhé.
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn hợp chất hữu cơ a thu được 4,4gam CO2 và 3,6gam H2O a)xác định công thức phân tử của a b) chất a có phản ứng đặc trưng nào mn giúp em với ạ
Dẫn 5,6 lít hỗn hợp khí metan và etilen (đktc) qua bình đựng dung dịch brom dư có 8 gam brom tham gia phản ứng. Thể tích mỗi khí trong hỗn hợp ban đầu lần lượt là (C=12, H=1, Br = 80)
Ta có: \(n_{Br_2}=\dfrac{8}{160}=0,05\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
_____0,05____0,05 (mol)
\(\Rightarrow V_{C_2H_4}=0,05.22,4=1,12\left(l\right)\)
\(V_{CH_4}=5,6-1,12=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
CH4 + Br2 ----x---->
C2H4 + Br2 ---------->C2H4Br2
nBr=m/M=8/160=0,05 (mol)
VC2H4=n.22,4= 0,05. 22,4=1,12(lít)
VCH4=5,6-1,12=4,48(lít)
Đúng 0
Bình luận (0)
Al2O3+HCl
Ni+HBrO3
Al2O3 + HCl ------>AlCl3+H2O
Ni+HBrO3 -------->Ni(BrO3)2+H2
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp gồm Na, Ba vào nước dư thu được dung dịch A và 4,48 lít H2(đktc). Thể tích dung dịch chứa đồng thời HCl 1M và H2SO4 0,5M cần để trung hòa dung dịch A là A. 100ml.B. 400ml.C. 200ml.D. 267ml.
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp gồm Na, Ba vào nước dư thu được dung dịch A và 4,48 lít H2(đktc). Thể tích dung dịch chứa đồng thời HCl 1M và H2SO4 0,5M cần để trung hòa dung dịch A là
A. 100ml.
B. 400ml.
C. 200ml.
D. 267ml.
Ta có: nOH- = 2nH2 = 0,4 (mol) = nH+
Gọi: V dd axit = a (l)
⇒ nH+ = a + 0,5.2.a = 0,4
⇒ a = 0,2 (l) = 200 (ml)
→ Đáp án: C
Đúng 1
Bình luận (0)
Phản ứng nào sau đây thuộc loại phản ứng trùng hợp (a C2H4+3O2-2CO2+2H2O) (b CH2=CH2+Br2-BrCH2-CH2Br)(c nCH2=CH2-(-CH2-CH2-)n)(dCH4+Cl2-CH3CL+HCL)ai giúp mik vs
đốt cháy 5,6 lít khí etilen. Hãy tính thể khí oxi và thể tích không khí cần dùng (các thể chất tích khí đo ở đktc) giải giúp mik zới ạ
Ta có: \(n_{C_2H_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
____0,25___0,75 (mol)
\(\Rightarrow V_{O_2}=0,75.22,4=16,8\left(g\right)\)
\(V_{kk}=\dfrac{V_{O_2}}{20\%}=84\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{C_2H_4}=\dfrac{5,6}{22,4}=0,25mol\\ C_2H_4+3O_2\xrightarrow[]{t^0}2CO_2+2H_2O\\ n_{O_2}=3n_{C_2H_4}=0,75mol\\ V_{O_2}=0,75.22,4=16,8l\\ V_{kk}=16,8:\dfrac{1}{5}=84l\)
Đúng 1
Bình luận (0)