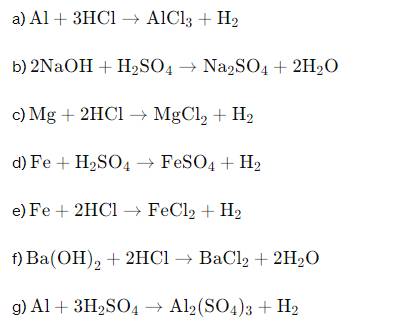Câu 1. Cho phương trình nhiệt hóa học của phản ứng: 3H2(g) + N2(g) -->2NH3(g) △rH298=-91,8kJ. Lượng nhiệt tỏa ra khi dùng 9 g H2(g) để tạo thành NH3(g) là bao nhiêu kJ?
Hóa học
\(n_{H_2}=9:2=4,5\left(mol\right)\)
Ta sẽ có sơ đồ sau:
3 mol H2->2NH3->\(\Delta_4H^0_{298}\)->-91,8kJ
=>4,5mol H2->-91,8x1,5=-137,7kJ
Đúng 0
Bình luận (0)
Câu 16. Các hợp chất hypochlorite hay Chlorine [NaClO, Ca(ClO)2] là các hóa chất có tính oxi hóa rất mạnh, có khả năng sát trùng, sát khuẩn, làm sạch nguồn nước (Chlorine được nhắc đến là tên thương mại, không phải đơn chất Cl2). Chlorine ở nồng độ xác định có khả năng tiêu diệt một số mầm bệnh như: E.coli, Hepatilis A virus, kí sinh trùng Giardia… và oxi hóa các chất khử trong nước như iron, manganese, hydrogen sulfide…Chlorine cần dùng là tổng lượng chlorine cần thiết để tiêu diệt mầm bệnh, ox...
Đọc tiếp
Câu 16. Các hợp chất hypochlorite hay Chlorine [NaClO, Ca(ClO)2] là các hóa chất có tính oxi hóa rất mạnh, có khả năng sát trùng, sát khuẩn, làm sạch nguồn nước (Chlorine được nhắc đến là tên thương mại, không phải đơn chất Cl2). Chlorine ở nồng độ xác định có khả năng tiêu diệt một số mầm bệnh như: E.coli, Hepatilis A virus, kí sinh trùng Giardia… và oxi hóa các chất khử trong nước như iron, manganese, hydrogen sulfide…
Chlorine cần dùng là tổng lượng chlorine cần thiết để tiêu diệt mầm bệnh, oxi hóa các chất khử trong nước và lượng chlorine tự do còn lại sau khoảng thời gian nhất định (mức chlorine tự do an toàn từ 0,1 đến 0,2 mg/l tại vòi sử dụng). Một nhà máy xử lí nước, muốn làm sạch 1 lít nước thì lượng chlorine cần dùng trong 1 ngày là 11 mg. Một ngày, nhà máy phải cung cấp 3000 m3 nước xử lí, thì lượng chlorine cần dùng là bao nhiêu kg?
Để tính lượng chlorine cần dùng cho việc xử lí nước, ta cần biết tổng lượng chlorine cần thiết cho 1 lít nước và sau đó áp dụng cho tổng lượng nước cần xử lí.
Theo đề bài, lượng chlorine cần dùng cho 1 lít nước là 11 mg. Ta cần chuyển đổi đơn vị từ mg sang kg để tính toàn bộ lượng chlorine cần dùng cho 3000 m³ nước.
1 mg = 1/1000 g = 1/1000000 kg.
Nên 11 mg = 11/1000000 kg = 0.000011 kg.
Tổng lượng chlorine cần dùng cho 3000 m³ nước là:
\[ 3000 \, \text{m}^3 \times 1000 \, \text{L/m}^3 \times 0.000011 \, \text{kg/L} = 33 \, \text{kg} \]
Vậy, nhà máy cần dùng 33 kg chlorine mỗi ngày để xử lí 3000 m³ nước.
Đúng 1
Bình luận (0)
Câu 15. Mưa lớn, kéo dài, nước ngập tràn, cuốn trôi rác thải và chất ô nhiễm trên mặt đất là một trong những nguyên nhân chính khiến nguồn nước bị ô nhiễm nghiêm trọng. Việc khử trùng nước ăn uống và sinh hoạt sau mỗi đợt lũ là hết sức cần thiết. Loại hóa chất được Bộ Y tế khuyến cáo sử dụng để xử lí nước sau lũ lụt là chloramine B được sử dụng dưới hai dạng là viên 0,25 gam và bột. Cứ 1 viên chloramine B có thể xử lý cho 25 lít nước ô nhiễm. Lưu ý rằng nước sau khi khử trùng vẫn cần đun sôi trư...
Đọc tiếp
Câu 15. Mưa lớn, kéo dài, nước ngập tràn, cuốn trôi rác thải và chất ô nhiễm trên mặt đất là một trong những nguyên nhân chính khiến nguồn nước bị ô nhiễm nghiêm trọng. Việc khử trùng nước ăn uống và sinh hoạt sau mỗi đợt lũ là hết sức cần thiết. Loại hóa chất được Bộ Y tế khuyến cáo sử dụng để xử lí nước sau lũ lụt là chloramine B được sử dụng dưới hai dạng là viên 0,25 gam và bột. Cứ 1 viên chloramine B có thể xử lý cho 25 lít nước ô nhiễm. Lưu ý rằng nước sau khi khử trùng vẫn cần đun sôi trước khi uống. Tính khối lượng (gam) chloramine B cần để khử trùng 3000 lít nước ô nhiễm trên?
giúp mình với , cách giải chi tiết ạ
Số Viên=3000/25=120 viên
Khối lượng chloramine B = Số viên . Khối lượng mỗi viên
= 120 viên. 0.25 gam/viên
= 30 gam
Vậy, cần khoảng 30 gam chloramine B để khử trùng 3000 lít nước ô nhiễm.
Đúng 1
Bình luận (0)
Câu 14. Một nhà máy nước cần sử dụng 5 mg Cl2 để làm sạch được 1 L nước sinh hoạt, công suất xử lý nước của nhà máy là 1000 m3/ngày. Tính khối lượng (gam) Cl2 nhà máy cần dùng trong 1 ngày để làm sạch nước theo đúng công suất?giúp mình gấp với , cần công thức cách giải cụ thể ạ !!!!
Đọc tiếp
Câu 14. Một nhà máy nước cần sử dụng 5 mg Cl2 để làm sạch được 1 L nước sinh hoạt, công suất xử lý nước của nhà máy là 1000 m3/ngày. Tính khối lượng (gam) Cl2 nhà máy cần dùng trong 1 ngày để làm sạch nước theo đúng công suất?
giúp mình gấp với , cần công thức cách giải cụ thể ạ !!!!
Bài Làm:
Đổi:
1 mg = 0.001 g.
Vậy, 5 mg Cl2 = 5 × 0.001 = 0.005 g Cl2.
Lượng Cl2 cần dùng cho 1 mét khối nước:
0.005 g Cl2 / 1 L nước
0.005 g Cl2/L nước × 1000 m³ = 5 g Cl2.
Vậy, nhà máy cần dùng 5 gam Cl2 trong mỗi ngày để xử lý nước theo công suất.
Đúng 1
Bình luận (2)
Viết phương trình hoàn thành chuỗi phản ứng hóa học sau ghi rõ điều kiện nếu có : CO2 -> CaCO3 -> CaO -> CaSO4 -> CaCO3
1.CO2 + Ca(OH)2 -> CaCO3 + H2O (Phản ứng tạo kết tủa canxi cacbonat trong nước) 2.CaCO3 -> CaO + CO2 (Phản ứng phân hủy canxi cacbonat thành vôi sống và khí cacbonic) 3. CaO + H2SO4 -> CaSO4 + H2O (Phản ứng tạo kết tủa canxi sunfat trong nước)4.CaSO4 + Na2CO3 -> CaCO3 + Na2SO4 (Phản ứng trao đổi ion giữa canxi sunfat và natri cacbonat tạo ra kết tủa canxi cacbonat và natri sunfat)
Đúng 0
Bình luận (0)
\(CO_2+CaO\rightarrow CaCO_3\downarrow\)
\(CaCO_3\rightarrow^{t^0}CaO+CO_2\)
\(CaO+H_2SO_4\rightarrow CaSO_4+H_2O\)
\(CaSO_4+Na_2CO_3\rightarrow CaCO_3\downarrow+Na_2SO_4\)
Đúng 0
Bình luận (0)
c1 Hoàn thành các pthh sau
a) Al+? ----> Alcl+H2
b)NaoH+?---->Na2So4+H2o
C)Mg+Hcl---->? +H2
D) ?+H2so4---->Fecl2 +H2
e) ?+Hcl ---->Fecl2+H2
F) Ba(OH)2+?---->Bacl2+H2o
g) ? +H2So4---->al2(so4)3 =H2
a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
c, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
d, \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
e, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
f, \(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
g, \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Đúng 1
Bình luận (0)
1- Đốt cháy hoàn toàn 4,6 gam một hợp chất A cần dùng vừa đủ V lít khí Oxygen (ở 25°C, áp suất I bar). Sau phản ứng thu được 8,8 gam CO2 và 5,4 gam H,O.
a) Tinh V.
b) Tìm công thức phân tử của A biết tỉ khối của A so với Hydrogen là 23.
a, BTKL, có: mA + mO2 = mCO2 + mH2O
⇒ mO2 = 8,8 + 5,4 - 4,6 = 9,6 (g)
\(\Rightarrow n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,3.24,79=7,437\left(l\right)\)
b, \(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,2.12 + 0,6.1 = 3 (g) < mA
→ A gồm C, H và O.
⇒ mO = 4,6 - 3 = 1,6 (g)
\(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,2:0,6:0,1 = 2:6:1
→ A có dạng (C2H6O)n
Mà: MA = 23.2 = 46 (g/mol)
\(\Rightarrow n=\dfrac{46}{12.2+6.1+16.1}=1\)
Vậy: A là C2H6O.
Đúng 1
Bình luận (0)
- Viết phương trình điều chế oxide
- trình bày được mối quan hệ giữa acid, base, oxide và muối ; rút ra được kết luận về tính chất hoá học của acid,base,oxide
- trình bày khái niệm thang pH, các giá trị của thang pH
- Khái niệm , công thức tính nồng độ mol, nồng độ dung dịch
Cho 6,952g KMnO4 tác dụng với 1 lượng dư dung dịch HCl đặc, khí clo tạo thành được dẫn đi chậm qua ống đựng 7,8g kim loại A(hóa trị không đổi) nung nóng. Kết thúc phản ứng, chia chất rắn thu được thành 2 phần bằng nhau : Phần I: Tác dụng với lượng dư dung dịch axít HCl làm thoát ra 112ml khí H2(đktc).
phần II: khuấy kĩ trong dung dịch AgNO3 dư thu được m gam kết tủa.
xác định kim loại A và tính m. Biết các phản ứng xảy ra hoàn toàn.
Đọc tiếp
Cho 6,952g KMnO4 tác dụng với 1 lượng dư dung dịch HCl đặc, khí clo tạo thành được dẫn đi chậm qua ống đựng 7,8g kim loại A(hóa trị không đổi) nung nóng. Kết thúc phản ứng, chia chất rắn thu được thành 2 phần bằng nhau : Phần I: Tác dụng với lượng dư dung dịch axít HCl làm thoát ra 112ml khí H2(đktc). phần II: khuấy kĩ trong dung dịch AgNO3 dư thu được m gam kết tủa. xác định kim loại A và tính m. Biết các phản ứng xảy ra hoàn toàn.
Trình bày bằng lời và viết phương trình hóa học (nếu có) Bằng phương pháp hóa học hãy nhận biết: a) 4 dung dịch không màu:NaOH, Na2SO4, H2SO4, HCl. b) 4 dung dịch không màu:NaCl, Ba(OH)2, NaOH, Na2SO4 (chỉ dùng quỳ tím).
a, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: Na2SO4
+ Quỳ hóa đỏ: H2SO4, HCl (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: H2SO4
PT: \(BaCl_2+H_2SO_4\rightarrow BaSO_{4\downarrow}+2HCl\)
+ Không hiện tượng: HCl.
- Dán nhãn.
b, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: Ba(OH)2, NaOH (1)
+ Quỳ không đổi màu: NaCl, Na2SO4 (2)
- Cho mẫu thử nhóm (1) và (2) pư lần lượt với nhau.
+ Có tủa trắng: nhóm (1) là Ba(OH)2, nhóm (2) là Na2SO4
PT: \(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\)
+ Còn lại là NaOH ở nhóm (1) và NaCl ở nhóm (2)
- Dán nhãn.
Đúng 0
Bình luận (0)